Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,4}{5}\Rightarrow O_2dư\)
\(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=\dfrac{5}{4}.0,2=0,25\left(mol\right)\\ n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(n_{P_2O_5\left(lt\right)}=\dfrac{1}{2}n_P=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2\left(g\right)\\ m_{P_2O_5\left(tt\right)}=0,1.142.80\%=11,36\left(g\right)\)

Sửa câu b: tính kl oxi đã dùng
\(a,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ b,\text{Bảo toàn KL: }m_P+m_{O_2}=m_{P_2O_5}\\ \Rightarrow m_{O_2}=7,1-3,1=4(g)\)

a.\(n_{CH_4}=\dfrac{V_{CH_4}}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,3 0,6 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,6.22,4=13,44l\)
b.
\(n_P=\dfrac{m_P}{M_P}=\dfrac{3,1}{31}=0,1mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,1 0,05 ( mol )
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=0,05.142=7,1g\)

\(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\\ n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\\ pthh:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,1}{4}>\dfrac{0,1}{5}\)
=> P dư
\(n_{P\left(p\text{ư}\right)}=\dfrac{4}{5}n_{O_2}=0,08\left(mol\right)\\
m_{P\left(d\right)}=\left(0,1-0,08\right).31=0,62\left(g\right)\)
\(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\\ n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
PTHH: \(4P+5O_2\xrightarrow[]{t^o}2P_2O_5\)
bđ 0,1 0,1
pư 0,08 0,1
spư 0,02 0
=> P dư
\(m_{P\left(dư\right)}=0,02.31=0,62\left(g\right)\)
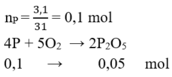
nP = 3,1/31 = 0,1 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
nP2O5 = 0,1/2 = 0,05 (mol)
mP2O5 = 0,05 . 142 = 7,1 (g)
=> B
7,1g