Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHHL 2Cu + O2 --to--> 2CuO
0,2<--0,1<-------0,2
=> mCu = 0,2.64 = 12,8 (g)
b) \(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
=> Vkk = 2,24 : 20% = 11,2 (l)
c) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,15}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,15<-0,15----->0,15
=> \(\left\{{}\begin{matrix}n_{Cu}=0,15\left(mol\right)\\n_{CuO\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\)
=> mA = 0,15.64 + 0,05.80 = 13,6 (g)
Bài làm:
Số mol đồng oxit (CuO) là:
$n_{CuO}$ = $\frac{m_{CuO}}{M_{CuO}}$ = $\frac{16}{80}$ = 0,2 (mol)
PTHH: 2Cu + $O_{2}$ --$t^{o}$--> 2CuO
Theo PT: 2 mol 1 mol <-- 2 mol
Theo bài: 0,2 mol 0,1 mol <-- 0,2 mol
a)Khối lượng đồng (Cu) là:
$m_{Cu}$ = $M_{Cu}$ . $n_{Cu}$ = 64. 0,2 = 12,8 (g)
b)Thế tích khí oxi ($O_{2}$) là:
$V_{O_{2}}$ = $n_{O_{2}}$ . 22,4 = 0,1 . 22,4 = 2,24 (lít)
Thể tích chiếm 20% thể tích không khí
=>$V_{kk}$ = 22,4 : 20% = 11,2 (lít)
c)Số mol khí hiđro ($H_{2}$) là:
$n_{H_{2}}$ = $\frac{m_{H_{2}}}{M_{H_{2}}}$ = $\frac{3,36}{22,4}$ = 0,15 (mol)
PTHH: CuO + H2 --to--> Cu + H2O
Theo PT: 1 mol 1 mol 1 mol 1 mol
Theo bài: 0,15 mol 0,15 mol 0,15 mol 0,15 mol
Xét tỉ lệ: $\frac{0,2}{1}$ > $\frac{0,15}{1}$
=> CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
Theo PT: 1 mol 1 mol 1 mol 1 mol
Theo bài: 0,15 mol 0,15 mol 0,15 mol 0,15 mol
Số mol đồng (Cu) là: 0,15 mol như PTHH
Số mol đồng (II) oxit (CuO) dư là: 0,05 mol tự tính
=> mA = 0,15.64 + 0,05.80 = 13,6 (g)
ok chưa nè
#Aria_Cortez

a)a)nMgO=\(\dfrac{32}{40}\)=0,8(mol)
PT:2Mg+O2to→2MgO
⇒nO2=\(\dfrac{0,8}{2}\)=0,4(mol)
⇒VO2=0,4.22,4=8,96(l)
⇒Vkk=8,96:20%=44,8(l)
b)b)nMg=nMgO=0,8(mol)
⇒mMg=24.0,8=19,2(g)
%mMg=\(\dfrac{19,2}{20}\).100%=96%
a) Số mol magie oxit là 32/40=0,8 (mol).
2Mg (0,8 mol) + O2 (0,4 mol) \(\underrightarrow{t^o}\) 2MgO (0,8 mol).
Thể tích không khí đủ dùng để đốt cháy là:
V=0,4.22,4:20%=44,8 (lít).
b) Khối lượng kim loại Mg đã phản ứng là 0,8.24=19,2 (g).
Phần trăm theo khối lượng của Mg trong mẩu kim loại nói trên:
%mMg=19,2/20=96%.

\(a.PTHH:2B+O_2\overset{t^o}{--->}2BO\left(1\right)\)
b. Áp dụng ĐLBTKL, ta có:
\(m_B+m_{O_2}=m_{BO}\)
\(\Leftrightarrow m_{O_2}=8-4,8=3,2\left(g\right)\)
c. Ta có: \(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,1.22,4=2,24\left(lít\right)\)
Mà: \(V_{O_2}=\dfrac{1}{5}.V_{kk}\)
\(\Leftrightarrow V_{kk}=2,24.5=11,2\left(lít\right)\)
d. Theo PT(1): \(n_B=2.n_{O_2}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow M_B=\dfrac{4,8}{0,2}=24\left(\dfrac{g}{mol}\right)\)
Vậy B là magie (Mg)
\(e.PTHH:2xB+yO_2\overset{t^o}{--->}2B_xO_y\left(2\right)\)
Theo PT(2): \(n_B=\dfrac{2x}{y}.n_{O_2}=\dfrac{2x}{y}.0,1=\dfrac{0,2x}{y}\left(mol\right)\)
\(\Rightarrow M_B=\dfrac{4,8}{\dfrac{0,2x}{y}}=\dfrac{4,8y}{0,2x}=12.\dfrac{2y}{x}\left(mol\right)\)
Biện luận:
| 2y/x | 1 | 2 | 3 |
| MB | 12 | 24 | 36 |
| loại | Mg | loại |
Vậy B là kim loại magie (Mg)

PTHH: \(2K+2H_2O\rightarrow2KOH+H_2\)
\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\)
Theo PTHH: \(n_{H_2}=\dfrac{1}{2}n_K=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
\(2H_2+O_2\xrightarrow[]{t^o}2H_2O\)
Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22.4=0,05.22,4=1,12\left(l\right)\)
Thể tích không khí đã dùng:
\(V_{kk}=\dfrac{V_{O_2}.100\%}{20\%}==5,6\left(l\right)\)
Mình cảm ơn bạn ạ bạn có thể cho mình hỏi thêm một bài nữa không ạ
Để đốt cháy 11,2g kim loại Fe trong khí Clo thủ được FeCl3
Tính thể tích khí Clo cần dùng cho phản ứng
Bạn giúp mình vs chiều nay ,1h mình thi ròi mà vẫn chưa biết làm bài này nhanh giúp mình vs ạ

\(a,PTHH:2Mg+O_2\xrightarrow{t^o}2MgO\\ b,BTKL:m_{O_2}=m_{MgO}-m_{Mg}=20-12=8(g)\\ \Rightarrow V_{O_2}=\dfrac{8}{32}.22,4=5,6(l)\\ \Rightarrow V_{kk}=\dfrac{5,6}{\dfrac{1}{5}}=28(l)\)

a) PTHH: \(4Al+3O_2\rightarrow2Al_2O_3\)
b) \(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{13,5}{27}=0,5\left(mol\right)\)
Theo PTHH: \(n_{Al_2O_3}=\dfrac{0,5.2}{4}=0,25\left(mol\right)\)
Khối lượng sản phẩm tạo thành: \(m_{Al_2O_3}=n_{Al_2O_3}.M_{Al_2O_3}=0,25.102=25,5\left(g\right)\)
c) Theo PTHH: \(n_{O_2}=\dfrac{0,5.3}{4}=0,375\left(mol\right)\)
Thể tích không khí cần dùng: \(V_{O_2}=n_{O_2}.22,4=0,375.22,4=8,4\left(l\right)\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}=\dfrac{2}{15}\left(mol\right)\Rightarrow V_{O_2}=\dfrac{2}{15}.22,4=\dfrac{224}{75}\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=\dfrac{224}{15}\left(l\right)\)
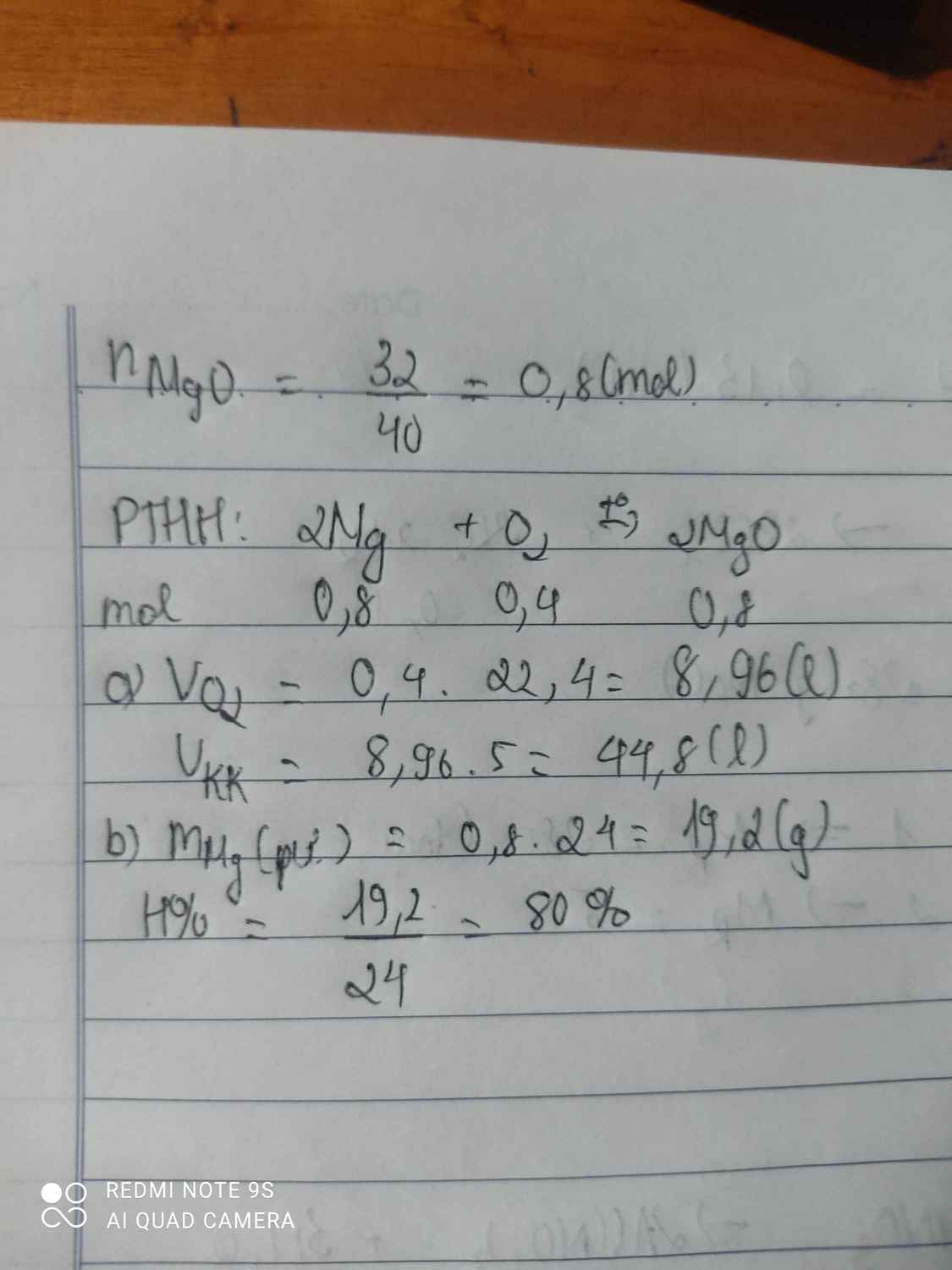
\(a,PTHH:4A+3O_2\underrightarrow{t^o}2A_2O_3\\ Áp.dụng.ĐLBTKL,ta.có:\\ m_A+m_{O_2}=m_{A_2O_3}\\ \Rightarrow m_{O_2}=m_{A_2O_3}-m_A=20,4-10,8=9,6\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{m}{M}=\dfrac{9,6}{32}=0,3\left(mol\right)\\ Theo.PTHH:n_A=\dfrac{4}{3}.n_{O_2}=\dfrac{4}{3}.0,3=0,4\left(mol\right)\\ \Rightarrow M_A=\dfrac{m}{n}=\dfrac{10,8}{0,4}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A.là.Al\left(nhôm\right)\)
\(b,V_{O_2\left(đktc\right)}=n.22,4=0,4.22,4=8,96\left(l\right)\\ \Rightarrow V_{kk\left(đktc\right)}=V_{O_2\left(đktc\right)}.5=8,96.5=44,8\left(l\right)\)
\(a,4A+3O_2\rightarrow\left(t^o\right)2A_2O_3\\ Theo.ĐLBTKL:\\ m_A+m_{O_2}=m_{A_2O_3}\\ \Leftrightarrow10,8+m_{O_2}=20,4\\ \Leftrightarrow m_{O_2}=9,6\left(g\right)\\ \Rightarrow n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\\ n_A=\dfrac{4}{3}.0,3=0,4\left(mol\right)\Rightarrow M_A=\dfrac{m_A}{n_A}=\dfrac{10,8}{0,4}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Nhôm\left(Al=27\right)\\ b,V_{kk\left(đktc\right)}=\dfrac{100}{20}.V_{O_2\left(đktc\right)}=5.\left(0,3.22,4\right)=33,6\left(l\right)\)