Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cu khong tác dụng với O2
=> nO2=6,72:22,4=0,3mol
PTHH: 3Fe+2O2=> Fe3O4
0,45mol<-0,3mol
=> mFe=0,45.56=25,2
=> m chất rắn là mCu= 29,6-25,2=4,4g

PTHH:
\(CuO+H_2\) \(\underrightarrow{t^o}\) \(Cu+H_2O\) \(\left(1\right)\)
\(Fe_2O_3+3H_2\) \(\underrightarrow{t^o}\) \(2Fe+3H_2O\) \(\left(2\right)\)
Số mol H2 là 0,6 mol
Gọi số mol H2 tham gia pư 1 là x mol \(\left(0,6>x>0\right)\)
Số mol H2 tham gia pư 2 là \(\left(0,6-x\right)mol\)
Theo PTHH 1:
\(n_{CuO}=n_{H_2}=x\left(mol\right)\)
Theo PTHH 2:
\(n_{Fe_2O_3}=\frac{1}{3}n_{H_2}=\left(0,6-x\right):3\left(mol\right)\)
Theo bài khối lượng hh là 40g
Ta có pt: \(80x+\left(0,6-x\right)160:3=40\)
Giải pt ta được \(x=0,3\)
Vậy \(n_{CuO}=0,3\left(mol\right);n_{Fe_2O_3}=0,1\left(mol\right)\)
\(\%m_{CuO}=\left(0,3.80.100\right):40=60\%\)
\(\%m_{Fe_2O_3}=\left(0,1.160.100\right):40=40\%\)
1)
PTHH: \(2Cu+O_2\) \(\underrightarrow{t^o}\) \(2CuO\)
x x
Gọi số mol Cu phản ứng là x mol ( x >0)
Chất rắn X gồm CuO và Cu
Ta có PT: 80x + 25,6 – 64x = 28,8
Giải PT ta được x = 0,2
Vậy khối lượng các chất trong X là:
\(m_{Cu}\) = 12,8 gam
\(m_{CuO}\) = 16 gam
2)
Gọi kim loại hoá trị II là A.
PTHH: \(A+2HCl\rightarrow ACl_2+H_2\)
Số mol \(H_2\)= 0,1 mol
Theo PTHH: \(n_A=n_{H_2}\)= 0,1 (mol)
Theo bài \(m_A\) = 2,4 gam \(\Rightarrow\) \(M_A\) = 2,4 : 0,1 = 24 gam
Vậy kim loại hoá trị II là Mg

\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Gọi x, y lần lượt là số mol của Cu, Fe
PTHH:
\(2Cu+O_2-t^o->2CuO\)
...x.........0,5x....................x
\(3Fe+2O_2-t^o->Fe_3O_4\)
..y...........\(\dfrac{2y}{3}\).....................\(\dfrac{y}{3}\)
Ta có hệ PT: \(\left\{{}\begin{matrix}64x+56y=29,6\\0,5x+\dfrac{2y}{3}=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
=> \(n_{CuO}=x=0,2\left(mol\right)\Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)
\(n_{Fe_3O_4}=\dfrac{y}{3}=\dfrac{0,3}{3}=0,1\left(mol\right)\Rightarrow m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)
\(\Rightarrow m_{chất-rắn}=m_{CuO}+m_{Fe_3O_4}=16+23,2=39,2\left(g\right)\)

Bài tập của bạn hình như là sai số nên mk tính ko ra.
nH2 = 1,68/22,4 = 0,075 mol
Fe (0,075) + 2HCl ------> FeCl2 + H2 (0,075)
-Theo PTHH: nFe = 0,075 mol
=> mFe= 0,075 . 56 = 4,2 gam
=> mCu = 8 - 4,2 = 3,8 gam

TN1: Gọi (nCu, nAl, nFe) = (a,b,c)
=> 64a + 27b + 56c = 14,3 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
b----------------------->1,5b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> 1,5b + c = 0,3 (2)
TN2: Gọi (nCu, nAl, nFe) = (ak,bk,ck)
=> ak + bk + ck = 0,6 (3)
\(n_{O_2}=\dfrac{44,8}{22,4}.20\%=0,4\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
ak--->0,5ak
4Al + 3O2 --to--> 2Al2O3
bk--->0,75bk
3Fe + 2O2 --to--> Fe3O4
ck-->\(\dfrac{2}{3}ck\)
=> 0,5ak + 0,75bk + \(\dfrac{2}{3}ck\) = 0,4 (4)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,1\left(mol\right)\\c=0,15\left(mol\right)\\k=2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,05.64}{14,3}.100\%=22,38\%\\\%m_{Al}=\dfrac{0,1.27}{14,3}.100\%=18,88\%\\\%m_{Fe}=\dfrac{0,15.56}{14,3}.100\%=58,74\%\end{matrix}\right.\)

a)
Theo ĐLBTKL: \(m_{Fe\left(bđ\right)}+m_{O_2}=m_X\)
=> \(m_{O_2}=26,4-20=6,4\left(g\right)\)
=> \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\Rightarrow V=0,2.22,4=4,48\left(l\right)\)
b)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,2------->0,1
=> \(\%m_{Fe_3O_4}=\dfrac{0,1.232}{26,4}.100\%=87,88\%\)
c)
- Nếu dùng KClO3
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{0,4}{3}\)<-----------------0,2
=> \(m_{KClO_3}=\dfrac{0,4}{3}.122,5=\dfrac{49}{3}\left(g\right)\)
- Nếu dùng KMnO4:
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,4<--------------------------------0,2
=> \(m_{KMnO_4}=0,4.158=63,2\left(g\right)\)

\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{Fe}=0,15\left(mol\right)\\ \Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\\ ChấtrắnkhôngtanlàCu\\ Cu+Cl_2\text{ }\rightarrow CuCl_2\\ n_{Cu}=n_{Cl_2}=0,2\left(mol\right)\\ \Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\\ \%m_{Fe}=\dfrac{8,4}{8,4+12,8}.100=39,62\%\\ \%m_{Cu}=100-39,62=60,38\%\)

a)
\(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2 (1)
0,6<----------------------0,3
=> mNa = 0,6.23 = 13,8 (g)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<-0,2
=> mFe = 0,1.56 = 5,6 (g)
mCu = 10 (g)
\(\left\{{}\begin{matrix}\%Na=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%Fe=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%Cu=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=\dfrac{17,4}{\dfrac{0,3}{y}}=58y\left(g/mol\right)\)
=> 56x = 42y
=> \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
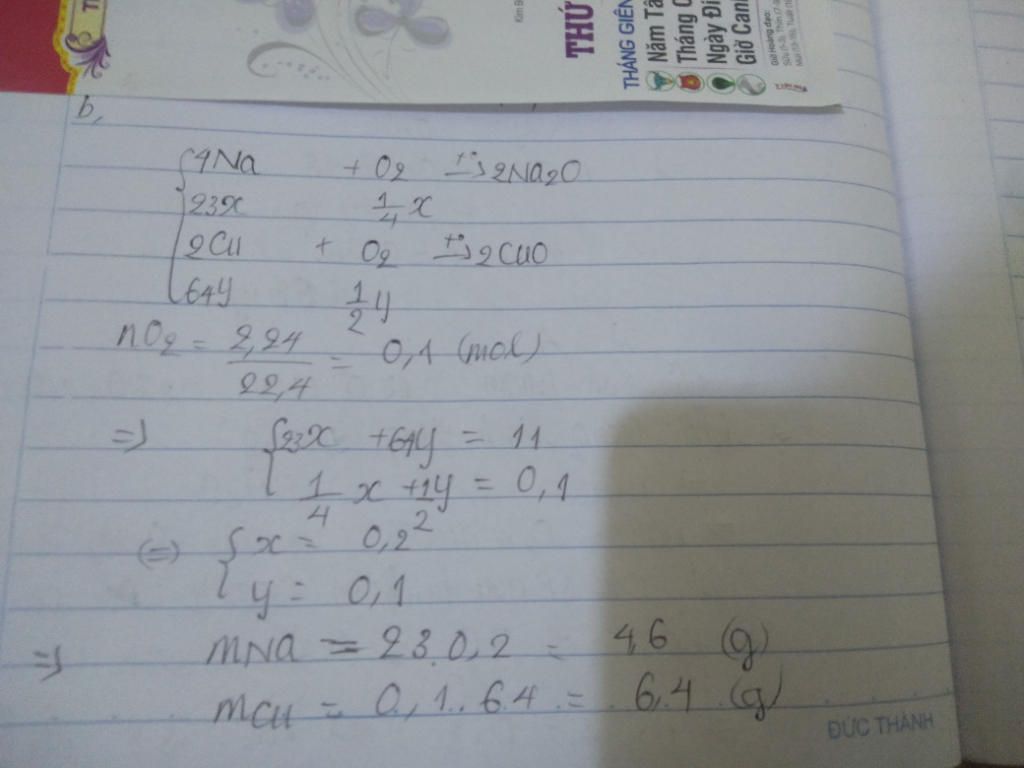
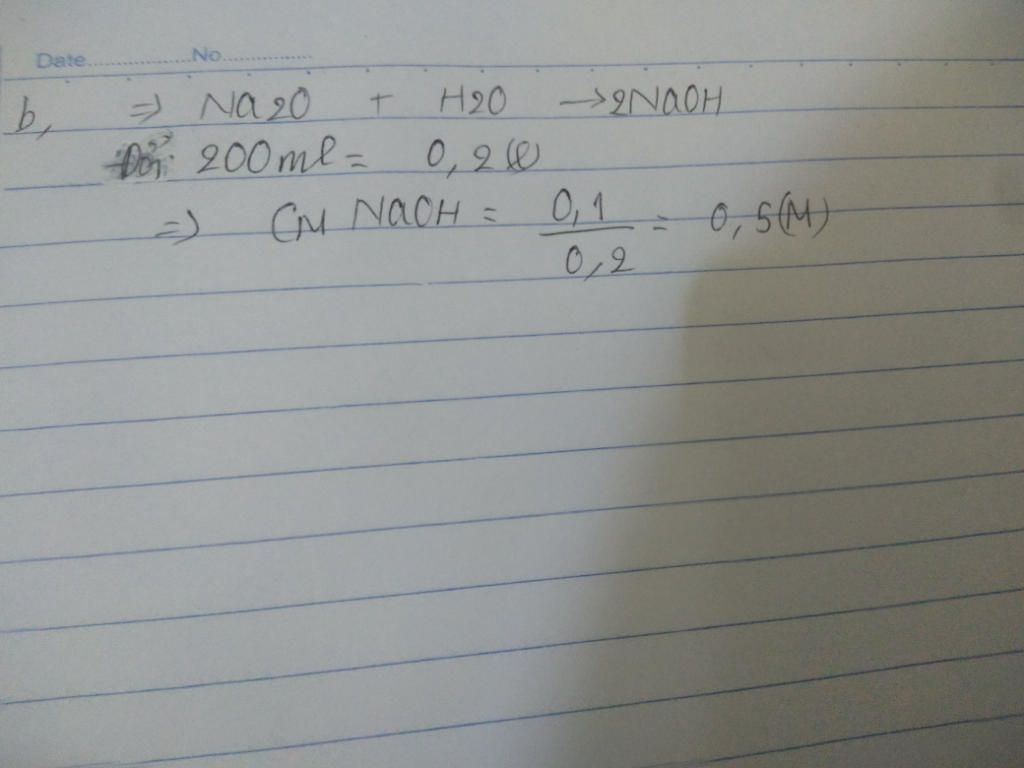
\(2Cu + O_2 \xrightarrow{t^o} 2CuO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ \text{Bảo toàn khối lượng : } \\ m_{rắn\ tạo\ thành} = m_{kim\ loại} + m_{O_2} = 29,6 + 0,3.32 = 39,2(gam)\)