Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có : nguyên tử khối trung bình của đồng được tính theo công thức :
63,54 = \(\frac{165+\left(100-a\right)63}{100}\)
Trong đó a là phần trăm số nguyên tử \(\frac{65}{29}Cu,q,\left(100-a\right)\) là phần trăm số nguyên tử \(\frac{63}{19}Cu\) . Giải ra ta có a = 27%
Vậy \(\frac{65}{29}Cu\) có 27% , \(\frac{63}{29}Cu\) có 73 %

gọi a là số khối của Y( số khối của Y lớn hơn của Z ) --> ta có số khối của Z là 128-a ta có sơ đồ đường chéo
Y (a) 63,54-(128-a)
Z (128-a) 63,54 a-63,54
từ số nguyên tử đồng vị Y = 0,37 lần số nguyên tử đồng vị Z. Xác định số khối của Y và Z.ta có
63,54-(128-a)=0,37*(a-63,54) sau đó giải a là xong chúc bạn học tốt

Đặt x nguyên tử khối của đồng vị còn lại
Ta có : \(\overline{M}=\dfrac{54,5.79+\left(100-54,5\right).x}{100}=79,91\)
\(\rightarrow x=81\)
Vậy nguyên tử khối của đồng vị còn lại : \(^{81}X\)

Ví dụ: Trong tự nhiên, chlorine có hai đồng vị bền là \(\overset{35}{17}\)Cl (chiếm 75,77%) và \(\overset{37}{17}\)Cl (chiếm 24,23%).
Ta xác định được:
- Đồng vị: \(\overset{35}{17}\)Cl và \(\overset{37}{17}\)Cl có nguyên tử khối lần lượt là 35 và 37.
- Nguyên tử trung bình của nguyên tố chlorine là
\(\overline{A}=\dfrac{35.75,77+37.23,37}{100}=35,16\)
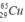
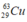
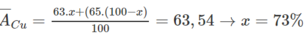
Gọi x là thành phần % của đồng vị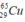
Ta có: