
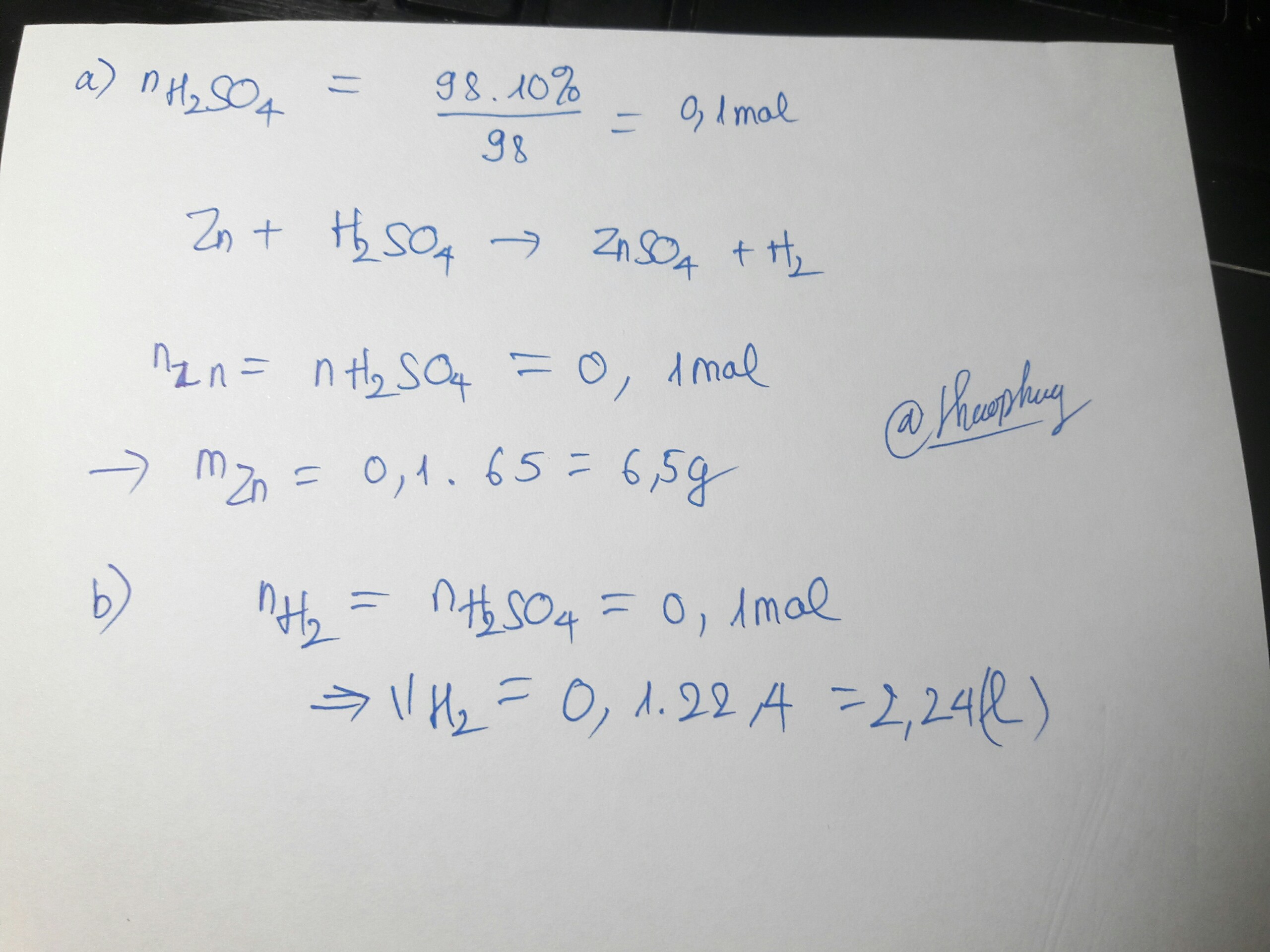
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

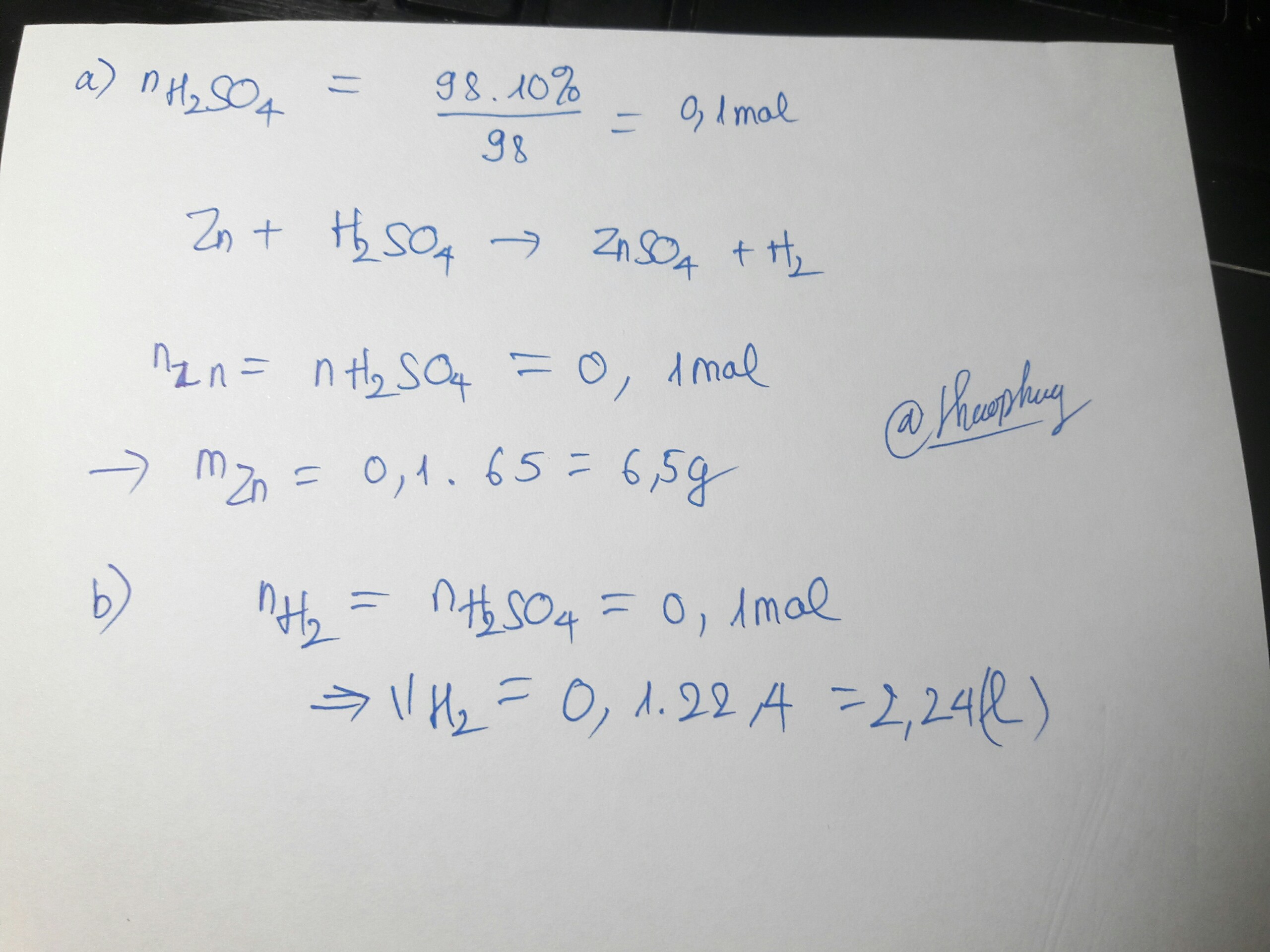

Mình thay trên câu a luôn nhé.
5. Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
a) Ta có PTHH :
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,1 mol 0,2 mol 0,1 mol 0,1 mol
Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
b) Khối lượng của FeCl2 tạo thành sau p.ứng là :
mFeCl2 = 0,1.127 = 12,7 (g)
c) Thể tích khí Hiđro (đktc) tạo thành sau p.ứng là :
VH2 = 0,1.22,4 = 2,24 (l)
4. Công thức của B là : NaxCyOz
+ \(m_{Na}=\frac{106.43,6}{100}\approx46\left(g\right)\)
\(m_C=\frac{106.11,3}{100}\approx12\left(g\right)\)
\(m_O=\frac{106.45,3}{100}\approx48\left(g\right)\)
+ \(n_{Na}=\frac{46}{23}=2\left(mol\right)\)
\(n_C=\frac{12}{12}=1\left(mol\right)\)
\(n_O=\frac{48}{16}=3\left(mol\right)\)
Suy ra trong một p.tử h/c có 2 n.tử Na, 1 n.tử C và 3 n.tử O.
\(\Rightarrow\) CTHH của hợp chất B là Na2CO3.

Bài 10:
- Giả sử có 100 gam dd H2SO4 98%
\(m_{H_2SO_4}=\dfrac{100.98}{100}=98\left(g\right)\) => \(n_{H_2SO_4}=\dfrac{98}{98}=1\left(mol\right)\)
\(V_{dd.H_2SO_4.98\%}=\dfrac{100}{1,84}=\dfrac{1250}{23}\left(ml\right)=\dfrac{5}{92}\left(l\right)\)
\(C_{M\left(dd.H_2SO_4.98\%\right)}=\dfrac{1}{\dfrac{5}{92}}=18,4M\)
\(n_{H_2SO_4}=18,4.0,05=0,92\left(mol\right)\)
=> \(m_{H_2SO_4}=0,92.98=90,16\left(g\right)\)
=> \(m_{dd.H_2SO_4.10\%}=\dfrac{90,16.100}{10}=901,6\left(g\right)\)
Bài 11:
a) Do dd sau pư có 3 chát tan với nồng độ % bằng nhau
=> \(m_{Al_2\left(SO_4\right)_3}=m_{ZnSO_4}=m_{H_2SO_4\left(dư\right)}\)
Gọi số mol Al, Zn là a, b (mol)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
a----->1,5a------->0,5a----->1,5a
Zn + H2SO4 --> ZnSO4 + H2
b----->b--------->b----->b
=> \(\left\{{}\begin{matrix}m_{Al_2\left(SO_4\right)_3}=342.0,5a=171a\left(g\right)\\m_{ZnSO_4}=161b\left(g\right)\end{matrix}\right.\)
=> 171a = 161b
=> \(\dfrac{a}{b}=\dfrac{161}{171}\) (1)
Có: \(\dfrac{m_{Al}}{m_{Zn}}=\dfrac{27.n_{Al}}{65.n_{Zn}}=\dfrac{27}{65}.\dfrac{161}{171}=\dfrac{483}{1235}\)
b) \(n_{H_2}=1,5a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{161}{825}\left(mol\right)\\b=\dfrac{57}{275}\left(mol\right)\end{matrix}\right.\)
=> \(x=\dfrac{161}{825}.27+\dfrac{57}{275}.65=\dfrac{5154}{275}\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=m_{Al_2\left(SO_4\right)_3}=342.0,5\dfrac{161}{825}=\dfrac{9177}{275}\left(g\right)\)
=> \(m_{H_2SO_4\left(bđ\right)}=98\left(1,5a+b\right)+\dfrac{9177}{275}=\dfrac{22652}{275}\left(g\right)\)
=> \(y=\dfrac{\dfrac{22652}{275}.100}{10}=\dfrac{45304}{55}\left(g\right)\)

nZn = 19,5/65 = 0,3 (mol)
nH2SO4 = 49/98 = 0,5 (mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
LTL: 0,3 < 0,5 => H2SO4 dư
nH2SO4 (phản ứng) = mZnSO4 = 0,3 (mol)
mH2SO4 (dư) = (0,5 - 0,3) . 98 = 19,6 (g)
mZnSO4 = 0,3 . 161 = 48,3 (g)
PTHH: CuO + H2 -> (t°) Cu + H2O
Mol: 0,3 <--- 0,3 ---> 0,3
mCu = 0,3 . 64 = 19,2 (g)

\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,2 0,2 0,2 0,2
a)\(V_{H_2}=0,2\cdot22,4=4,48l\)
b)\(m_{ZnSO_4}=0,2\cdot161=32,2g\)
\(m_{ddZnSO_4}=30+200-0,2\cdot2=229,6g\)
\(C\%=\dfrac{m_{ct}}{m_{dd}}\cdot100\%=\dfrac{32,2}{229,6}\cdot100\%=14,02\%\)
c)\(n_{CuO}=\dfrac{24}{80}=0,3mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,3 0,2 0,2
\(m_{rắn}=m_{Cu}=0,2\cdot64=12,8g\)
nZn=1365=0,2molnZn=1365=0,2mol
Zn+H2SO4→ZnSO4+H2Zn+H2SO4→ZnSO4+H2
0,2 0,2 0,2 0,2
a)VH2=0,2⋅22,4=4,48lVH2=0,2⋅22,4=4,48l
b)mH2SO4=0,2⋅98=19,6gmH2SO4=0,2⋅98=19,6g
C%=mctmdd⋅100%=19,6200⋅100%=9,8%C%=mctmdd⋅100%=19,6200⋅100%=9,8%
c)nCuO=2480=0,3molnCuO=2480=0,3mol
CuO+H2→Cu+H2OCuO+H2→Cu+H2O
0,3 0,2 0,2
mrắn=mCu=0,2⋅64=12,8g.

a) Do dd sau pư có 3 chát tan với nồng độ % bằng nhau
=> \(m_{Al_2\left(SO_4\right)_3}=m_{ZnSO_4}=m_{H_2SO_4\left(dư\right)}\)
Gọi số mol Al, Zn là a, b (mol)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
a----->1,5a------->0,5a----->1,5a
Zn + H2SO4 --> ZnSO4 + H2
b----->b--------->b----->b
=> \(\left\{{}\begin{matrix}m_{Al_2\left(SO_4\right)_3}=342.0,5a=171a\left(g\right)\\m_{ZnSO_4}=161b\left(g\right)\end{matrix}\right.\)
=> 171a = 161b
=> \(\dfrac{a}{b}=\dfrac{161}{171}\) (1)
Có: \(\dfrac{m_{Al}}{m_{Zn}}=\dfrac{27.n_{Al}}{65.n_{Zn}}=\dfrac{27}{65}.\dfrac{161}{171}=\dfrac{483}{1235}\)
b) \(n_{H_2}=1,5a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{161}{825}\left(mol\right)\\b=\dfrac{57}{275}\left(mol\right)\end{matrix}\right.\)
=> \(x=\dfrac{161}{825}.27+\dfrac{57}{275}.65=\dfrac{5154}{275}\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=m_{Al_2\left(SO_4\right)_3}=342.0,5\dfrac{161}{825}=\dfrac{9177}{275}\left(g\right)\)
=> \(m_{H_2SO_4\left(bđ\right)}=98\left(1,5a+b\right)+\dfrac{9177}{275}=\dfrac{22652}{275}\left(g\right)\)
=> \(y=\dfrac{\dfrac{22652}{275}.100}{10}=\dfrac{45304}{55}\left(g\right)\)

a) Do dd sau pư có 3 chát tan với nồng độ % bằng nhau
=> \(m_{Al_2\left(SO_4\right)_3}=m_{ZnSO_4}=m_{H_2SO_4\left(dư\right)}\)
Gọi số mol Al, Zn là a, b (mol)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
a----->1,5a------->0,5a----->1,5a
Zn + H2SO4 --> ZnSO4 + H2
b----->b--------->b----->b
=> \(\left\{{}\begin{matrix}m_{Al_2\left(SO_4\right)_3}=342.0,5a=171a\left(g\right)\\m_{ZnSO_4}=161b\left(g\right)\end{matrix}\right.\)
=> 171a = 161b
=> \(\dfrac{a}{b}=\dfrac{161}{171}\) (1)
Có: \(\dfrac{m_{Al}}{m_{Zn}}=\dfrac{27.n_{Al}}{65.n_{Zn}}=\dfrac{27}{65}.\dfrac{161}{171}=\dfrac{483}{1235}\)
b) \(n_{H_2}=1,5a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{161}{825}\left(mol\right)\\b=\dfrac{57}{275}\left(mol\right)\end{matrix}\right.\)
=> \(x=\dfrac{161}{825}.27+\dfrac{57}{275}.65=\dfrac{5154}{275}\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=m_{Al_2\left(SO_4\right)_3}=342.0,5\dfrac{161}{825}=\dfrac{9177}{275}\left(g\right)\)
=> \(m_{H_2SO_4\left(bđ\right)}=98\left(1,5a+b\right)+\dfrac{9177}{275}=\dfrac{22652}{275}\left(g\right)\)
=> \(y=\dfrac{\dfrac{22652}{275}.100}{10}=\dfrac{45304}{55}\left(g\right)\)

a, PTPƯ: SO3 + H2O ---> H2SO4
nSO3=\(\dfrac{2,24}{22,4}=0,1mol\)
1 mol SO3 ---> 0,1 mol H2SO4
nên 0,1 mol SO3 ---> 0,1 mol H2SO4
CM H2SO4=\(\dfrac{0,1}{0,5}\)=0,2 M
b, PTPƯ: Zn + H2SO4 ---> ZnSO4 + H2
1 mol H2SO4 ---> 1 mol Zn
nên 0,1 mol H2SO4 ---> 0,1 mol Zn
mZn=0,1.65=6,5 g

nH2SO4 = 49/98 = 0.5 (mol)
CMH2SO4 = 0.5/0.15 = 3.3 (M)
Zn + H2SO4 => ZnSO4 + H2
...........0.5.............0.5.........0.5
VH2 = 0.5 * 22.4 = 11.2 (l)
CMZnSO4 = 0.5 / 0.15 = 10/3 (M)
C%ZnSO4 = CM*M / 10D = 10/3 * 161 / 10 * 1.25 = 42.9 %

a) PTHH : \(FeO+H_2-t^o->Fe+H_2O\)
\(CuO+H_2-t^o->Cu+H_2O\)
Đặt \(\hept{\begin{cases}n_{FeO}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{cases}}\) => \(72x+80y=11,2\left(I\right)\)
Có : \(m_{O\left(lấy.đi\right)}=m_{giảm}=1,92\left(g\right)\)
=> \(n_{O\left(lấy.đi\right)}=\frac{1,92}{16}=0,12\left(mol\right)\) Vì H% = 80% => Thực tế : \(n_{O\left(hh\right)}=\frac{0,12}{80}\cdot100=0,15\left(mol\right)\)
BT Oxi : \(x+y=0,15\left(II\right)\)
Từ (I) và (II) suy ra : \(\hept{\begin{cases}x=0,1\\y=0,05\end{cases}}\)
=> \(\hept{\begin{cases}m_{FeO}=7,2\left(g\right)\\m_{CuO}=4\left(g\right)\end{cases}}\)
b) PTHH : \(Fe+H_2SO_4-->FeSO_4+H_2\)
BT Fe : \(n_{Fe}=n_{FeO}=0,1\left(mol\right)\)
Theo pthh : \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(V_{H_2}=2,24\left(l\right)\)
BT Cu : \(n_{Cu}=n_{CuO}=0,05\left(mol\right)\)
=> \(m_{CR\left(ko.tan\right)}=0,05\cdot64=3,2\left(g\right)\)