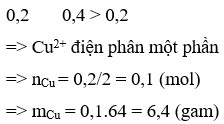Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
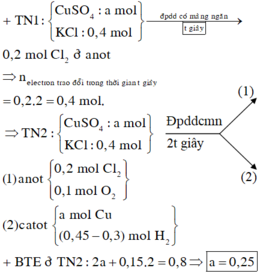
Thứ tự các phản ứng điện phân xảy ra:
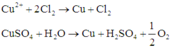
Do đó kim loại bám vào catot là Cu, khí thoát ra ở anot là Cl2, có thể có O2.
![]()
Áp dụng định luật bảo toàn mol electron, ta có:
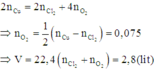

Đáp án A
- Khí bắt đầu thoát ra ở catot là khi Fe3+, Cu2+ bị điện phân hết, H+ vừa bị điện phân
Phương trình điện phân:
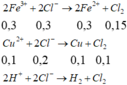
- Thêm dung dịch AgNO3 vừa đủ vào
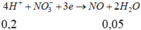
=> m Y =200+250-156,65-30.0,05-71.0,25=274,1 g
- Dung dịch Y Chứa 2 muối là: Fe(NO3)3 ; Cu(NO3)2
Muối có phân tử khối lớn hơn là Fe(NO3)3
C % Fe ( NO 3 ) 3 = 242 . 0 , 3 274 , 1 . 100 % = 26 , 49 % gần với giá trị 27 phút

Đáp án B
* t giây: n khí(anot) > 0,5nKCl => H2O bị điện phân
nCl2 = 0,5nKCl = 0,0375 mol
nO2 = 0,05-0,0375 = 0,0125 mol
n e(1) = 2nCl2 + 4nO2 = 0,0375.2 + 0,0125.4 = 0,125 mol
* 2t giây: n e(2) = 2ne(1) = 0,25 mol
n khí = 2,38/22,4 = 0,10625 mol
Catot:
Cu2+ +2e → Cu
a….....2a
H2O + 1e → OH- + 0,5H2
0,05← 0,025
Anot:
Cl- - 1e → 0,5Cl2
0,075..0,075..0,0375
H2O -2e → 2H+ + 0,5O2
0,175 0,04375
=> 2a + 0,05 = 0,25 => a = 0,1 mol