Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Ở anot xảy ra sự oxi hóa nước: 2H2O → 4H+ + O2 + 4e
nO2 = 0,01 => ne = 0,04
Mà ne = I.t/96500 => t = 0,04.96500/10 = 386 giây = 6 phút 26 giây

Đáp án A
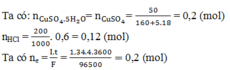
Thứ tự điện phân tại catot và anot là:
Tại catot: Cu2+ + 2e → Cu
0,1 0,2 0,1
⟹ Cu2+ chưa bị điện phân hết.
⟹ mkim loại ở catot = 0,1.64 = 6,4 (gam)
Tại anot: 2Cl– → Cl2 + 2e
0,12 0,06 0,12
⟹ ne (do Cl– nhường) = 0,12 < 0,2 mol
⟹ tại anot Cl– đã bị điện phân hết và đến nước bị điện phân.
Ta có: ne (do H2O nhường) = 0,2 – 0,12 = 0,08 (mol)
2H2O → O2 + 4H + 4e
0,02 ⟵ 0,08
Vkhí thoát ra ở anot = (0,06 + 0,02).22,4 = 1,792 (lít).

Đáp án C
Ta có n N a C l = 0 , 18 mol
Trong thời gian t giây ở anot thu được 0,15 mol khí trong đó có 0,09 mol Cl2 và còn lại là O2 0,06 mol.
→ n e = 0,09.2 + 0,06.4 = 0,42 mol
Khi thời gian điện phân là 2 t giây → n e = 0.84 mol
Vậy ở anot thu đươc 0,09 mol Cl2 và 0,165 mol O2.
Vậy ở catot thu được H2 0,17 mol.
Bảo toàn e:

= n M S O 4 . 5 H 2 O
Vậy M là Ni (59).
Tại thời gian t giây ta thu được ở catot là 0,21 mol Ni => m = 12,39 gam

Đáp án A
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+chưa điện phân hết
Tại t (s):
Catot: Cu2+ + 2e → Cu
0,16 ←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu Anot: 2Cl- → Cl2 + 2e
0,36 ←0,18 2x x 2x
2H2O + 2e → 2OH- + H2. 2H2O → 4H+ + O2 + 4e
2y→4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)

Đáp án A
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+chưa điện phân hết
Tại t (s):
Catot: Cu2++2e→Cu
0,16←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu
Anot: 2Cl- → Cl2 + 2e
0,36←0,18
2H2O + 2e → 2OH- + H2.
2x x 2x
2H2O → 4H+ +O2 + 4e
2y → 4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)

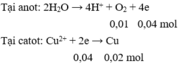

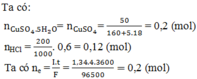


Đáp án A
Ta có:
Ta có quá trình xảy ra tại các điện cực:
Catot Anot
0,08 → 0,16 0,01 → 0,04
Nhận thấy: chưa điện phân hết
chưa điện phân hết
Bảo toàn electron ta có: n C u = 1 2 n e n h ậ n = 0 , 02 m o l → m c a t o t t ă n g = m C u = 0 , 02 . 64 = 1 , 28 g