Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Tại anot có khí Cl2 và O2 thoát ra với
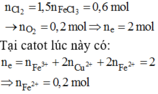
Dung dịch còn lại sau khi lấy catot ra khỏi bình điện phân chứa Fe2+ dư (0,2 mol); H+ (0,8 mol); NO3– (1,2 mol), lúc này tiếp tục xảy ra phản ứng oxi hóa khử nên n H + dư = 0,8 – 4 3 n F e + =8/15 mol
Dung dịch Y chứa Fe3+ (0,2 mol); H+ dư (8/15 mol) và NO3– (1,2 mol). Vậy m X - m Y = 91 , 67

Đáp án : D
nCl- = 0,4 mol => nCl2 = 0,2 mol < n khí anot = 0,4 mol
=> Có điện phân nước ở anot
| Catot Fe3+ + 1e à Fe2+ 0,4 0,4 0,4 Cu2+ + 2e à Cu 0,6 1,2 0,6 2H+ + 2e à H2 0,4 0,4 |
Anot 2Cl- à Cl2 + 2e 1,2 0,6 1,2 2H2O à 4H+ + O2 + 4e 0,8 0,2 0,8 |
=> Còn 0,4 mol Fe2+ ; 0,4 mol H+
3Fe2+ + 4H+ +NO3- è 3Fe3+ + NO + 2H2O
=> nNO = 0,1 mol ( Tính theo H+)
=> mX – mY = mCl2 + mCu + mH2 + mO2 + mNO = 90,8g

Catot: F e 3 + + e → F e 2 +
C u 2 + + 2 e → → C u
F e 2 + + 2 e → F e
· Anot: 2 C l - → C l 2 + 2 e
2 H 2 O → 4 H + + O 2 + 4 e
· nkhí anot = 17 , 92 22 , 4 = 0 , 8 m o l > n C l 2 = 0 , 6 m o l
=> Chứng tỏ ở anot đã xảy ra điện phân H2O.
n o 2 = 0 , 8 - 0 , 6 = 0 , 2 m o l , ne điện phân = 2 . 0 , 6 + 4 . 0 , 2 = 2 mol
· 0,4 + 2.0,6 < 2 < 0,4 + 2.0,6 + 2.0,4
=> Chứng tỏ Fe2+ chưa bị điện phân hết:
n F e đ i ệ n p h â n = 2 - 0 , 4 - 2 . 0 , 6 2 = 0 , 2 mol
· Phản ứng sau điện phân:
3Fe2+ + 4H+ + H N O 3 - → 3Fe3+ + NO + 2H2O
0,2 → 0 , 8 3 0 , 2 3 0,2 0 , 2 3 mol
=> mdư X - mdư Y = m C l 2 + m O 2 + + m C u + m F e + m N O
= 71 . 0 , 6 + 32 . 0 , 2 + 64 . 0 , 6 + 56 . 0 , 2 + 30 . 0 , 2 3 = 100 , 6 g
Gần nhất với giá trị 102.
=> Chọn đáp án B.
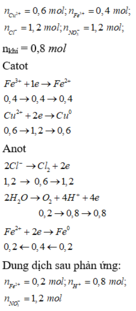







Khi trộn dung dịch ta có phương trình:
3Fe2+ + 4H+ + NO3− → 3Fe3+ + 2H2O + NO
0,2 0,4 1,2 → 0 , 2 3