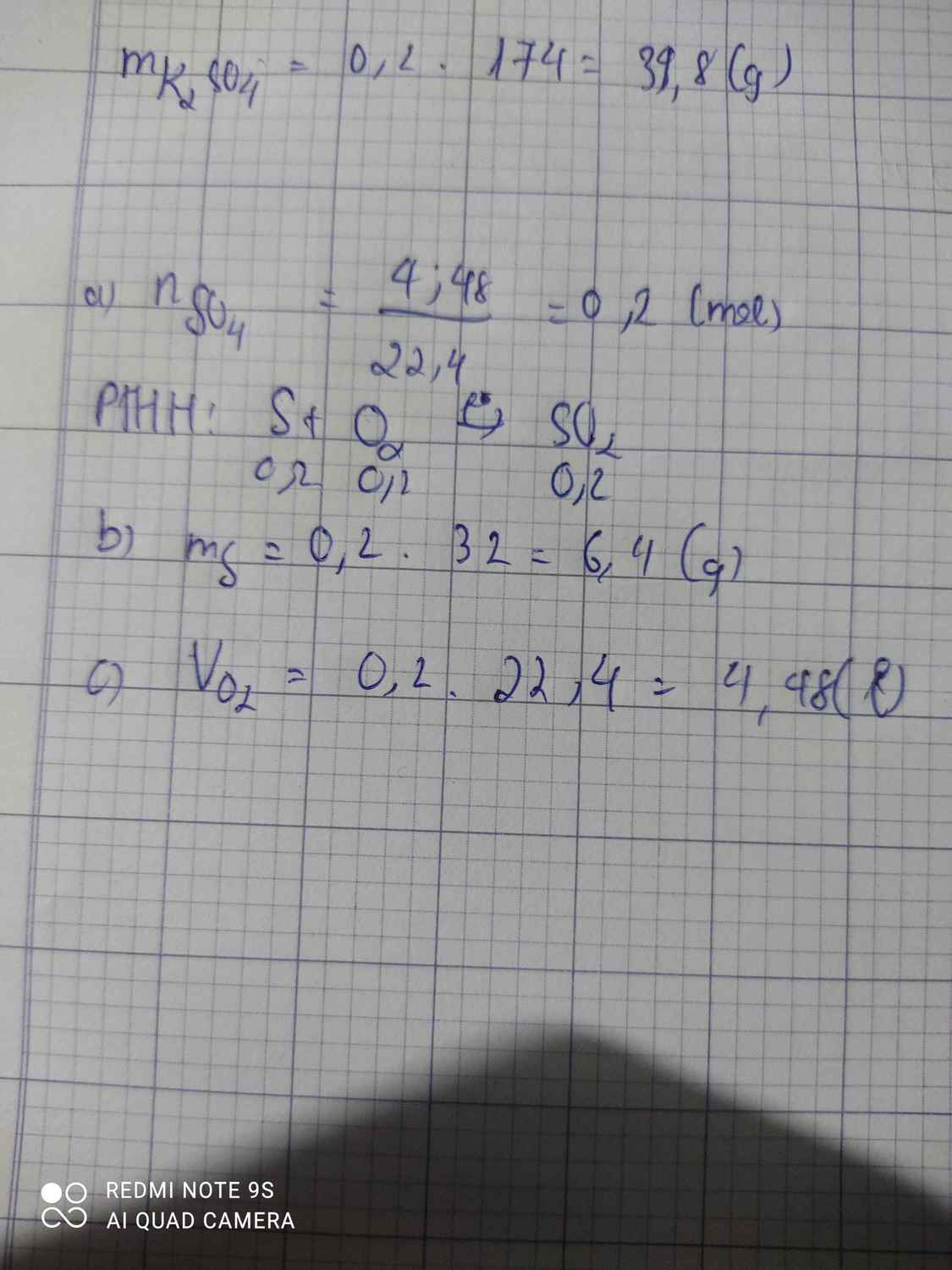Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{SO_3}=\dfrac{3}{80}=0,0375\left(mol\right)\\ pthh:SO_3+H_2O\rightarrow H_2SO_4\)
b) sản phẩm làm QT hóa đỏ vì sp là axit
\(pthh:SO_3+H_2O\rightarrow H_2SO_4\)
0,0375 0,0375
\(\Rightarrow m_{H_2SO_4}=0,0375.98=3,675\left(g\right)\)
\(C_M=\dfrac{0,0375}{0,25}=0,15M\)

S+O2-to>SO2
0,2--0,2----0,2 mol
n SO2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m S=0,2.32=6,4g
=>VO2=0,2.22,4=4,48l

a) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
b) nAl = \(\frac{40,5}{27}=1,5\left(mol\right)\)
Từ PT \(\Rightarrow n_{H_2SO_4}=2,25\left(mol\right);n_{Al_2\left(SO_4\right)_3}=0,75\left(mol\right);n_{H_2}=2,25\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=2,25.98=220,5\left(g\right)\)
c) \(m_{Al_2\left(SO_4\right)_3}=0,75.342=256,5\left(g\right)\)
d) đktc : \(V_{H_2}=22,4.2,25=50,4\left(l\right)\)
a) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 (1)
b) nAl = 40,5 : 27 = 1,5 mol
Từ pt(1) suy ra : nH2SO4 = \(\frac{3}{2}nAl\) = \(\frac{3}{2}.1,5=2,25mol\)
Khối lượng H2SO4 là : mH2SO4 = 2,25 . 98 = 220,5 g
c) Từ pt(1) => nAl2(SO4)3 = \(\frac{1}{2}nAl=\frac{1}{2}.1,5=0,75mol\)
=> mAl2(SO4)3 = 0,75 . 342 = 256,5 g
d) Từ pt(1) => nH2 = nH2SO4 = 2,25 mol
Thể tích khí H2 là : VH2=2,25 . 22,4 = 50,4 lit

Oxit tác dụng với nước: SO3, K2O, CaO, P2O5
- SO3 + H2O --> H2SO4
- K2O + H2O --> 2KOH
- CaO + H2O --> Ca(OH)2
P2O5 + 3H2O --> 2H3PO4
Không được nha cậu ơiii, chỉ có các oxit tan trong nước mới phản ứng được với nước thui, CuO với Al2O3 k phản ứng đc. Với lại CO đâu có tác dụng đc với nước âu

a, \(S+O_2\underrightarrow{^{to}}SO_2\)
b, \(n_{SO2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_S=n_{SO2}=0,2\left(mol\right)\)
\(\rightarrow m_S=0,2.32=64\left(g\right)\)
c, \(n_{O2}=n_{SO2}=0,2\left(mol\right)\)
\(\rightarrow V_{O2}=0,2.22,4=4,48\left(l\right)\)

a) Mg + H2SO4 --> MgSO4 + H2
b) \(n_{Mg}=\dfrac{3}{24}=0,125\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,125->0,125-->0,125-->0,125
=> VH2 = 0,125.22,4 = 2,8 (l)
\(V_{dd.H_2SO_4}=\dfrac{0,125}{2}=0,0625\left(l\right)\)
c) Sản phẩm là Magie sunfat và khí hidro
\(m_{MgSO_4}=0,125.120=15\left(g\right)\)
mH2 = 0,125.2 = 0,25 (g)
d)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,125}{1}\) => Hiệu suất tính theo H2
Gọi số mol CuO bị khử là a (mol)
PTHH: CuO + H2 --to--> Cu + H2O
a--->a-------->a
=> 16 - 80a + 64a = 14,4
=> a = 0,1 (mol)
=> nH2(pư) = 0,1 (mol)
=> \(H=\dfrac{0,1}{0,125}.100\%=80\%\)

a) \(n_{SO_3}=\dfrac{m}{M}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: `SO_3 + H_2O -> H_2SO_4`
b) Theo PTHH: `n_{H_2SO_4} = n_{SO_3} = 0,4 (mol)`
`=> m_{H_2SO_4} = 0,4.98 = 39,2 (g)`

a) S + O2 --to--> SO2
b) \(n_{SO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,5<-0,5<----0,5
=> \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
c) \(m_S=0,5.32=16\left(g\right)\)

a, \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: S + O2 ----to----> SO2
Mol: 0,2 0,2 0,2
b, \(m_{SO_2}=0,2.64=12,8\left(g\right)\)
c, \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)