Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Đặt:n_{C_2H_4}=a\left(mol\right);n_{C_3H_6}=b\left(mol\right)\left(a,b>0\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_3H_6+Br_2\rightarrow C_3H_6Br_2\\ m_{tăng}=m_{hh.ban.đầu}=7,7\left(g\right)\\ \Rightarrow Hpt:\left\{{}\begin{matrix}28a+42b=7,7\\a+b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,15\end{matrix}\right.\)
Vì thể tích tỉ lệ thuận với số mol nên ta có:
\(\%V_{C_2H_4\left(đktc\right)}=\%n_{C_2H_4}=\dfrac{a}{a+b}.100\%=\dfrac{0,05}{0,2}.100=25\%\\ \Rightarrow\%V_{C_3H_6}=100\%-25\%=75\%\)

Khi dẫn X qua AgNO3/NH3 thì chỉ có propin phản ứng
CHΞC-CH3 + AgNO3 + NH3 → AgCΞC-CH3 ↓ + NH4NO3
nAgCΞC-CH3 = \(\dfrac{29,4}{147}\)= 0,2 mol = nPropin
Nếu dẫn X qua bình đựng dd brom dư thì khối lượng bình tăng = mPropin + m Etilen
<=> 12,2 = mPropin + m Etilen
<=> 0,2.40 + mEtilen = 12,2
<=> mEtilen = 4,2 gam => nEtilen = 4.2:28 = 0,15 mol
nX = 10,08 : 22,4 = 0,45 mol
=> %V Etilen = \(\dfrac{0,15}{0,45}\).100% = 33,33%
%V Propin = \(\dfrac{0,2}{0,45}\).100% = 44,44%
=> %V Metan = 100 - 33,33 - 44,44 = 22,23%

- Gọi số mol etan là x ; số mol etilen là y. Ta có hệ phương trình :
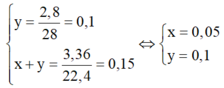
- Chọn đáp án A.

Dẫn X qua bình đựng Brom dư không thấy có khí thoát ra khỏi bình suy ra cả 2 hidrocacbon trong X đều có thể cộng brom
Tính được
![]()
Số liên kết pi trung bình:
![]()
Suy ra trong X có 1 anken và 1 hidrocacbon có ![]() (dựa vào 4 đáp án cũng có thể suy trong X có 1 anken, 1 ankin (ankadien))
(dựa vào 4 đáp án cũng có thể suy trong X có 1 anken, 1 ankin (ankadien))
Gọi công thức 2 hidrocacbon trên là![]() và
và ![]() với số mol tương ứng là x và y ta được:
với số mol tương ứng là x và y ta được:
![]()
Mặt khác khi đốt cháy X thu được 7,7 gam CO2
![]() hay n + 2m = 7
hay n + 2m = 7
Giải phương trình nghiệm nguyên này ta chỉ có n = 3; m = 2 thỏa mãn
Vậy 2 hidrocacbon cần tìm là C2H2 và C3H6
Đáp án B.
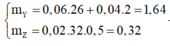
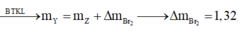
dẫn hỗn hợp trên qua dung dịch nước brom dư thì chỉ có etilen phản ứng nên khối lượng bình brom tăng là khối lượng của etilen
\(\Rightarrow\) m\(_{C_2H_4}\)= 5,6 (gam)
\(\Rightarrow\) n\(_{C_2H_4}\) = 5,6/28 = 0,2 (mol)
n\(_{hh}\) = \(\dfrac{6,72}{22,4}\) = 0,3 (mol)
Vậy %n\(_{C_2H_4}\) = \(\dfrac{0,2}{0,3}\)*100% \(\sim\) 66,7(%)
%V\(_{CH_4}\) = 100% - 66,7% = 33,3(%)