Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

250ml = 0,25l
\(n_{H2SO4}=1,5.0,25=0,375\left(mol\right)\)
\(n_{Na2SO3}=\dfrac{37,8}{126}=0,3\left(mol\right)\)
a) Pt : \(H_2SO_4+Na_2SO_3\rightarrow Na_2SO_4+SO_2+H_2O|\)
1 1 1 1 1
0,375 0,3 0,3 0,3
b) Lập tỉ số so sánh : \(\dfrac{0,375}{1}>\dfrac{0,3}{1}\)
⇒ H2SO4 dư , Na2SO3 phản ứng hết
⇒ Tính toán dựa vào số mol của Na2SO3
\(n_{SO2}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
c) \(n_{Na2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(n_{H2SO4\left(dư\right)}=0,375-0,3=0,075\left(mol\right)\)
\(C_{M_{Na2SO4}}=\dfrac{0,3}{0,25}=1,2\left(M\right)\)
\(C_{M_{H2SO4\left(dư\right)}}=\dfrac{0,075}{0,25}=0,3\left(M\right)\)
Chúc bạn học tốt

\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
_____0,2---->0,2------>0,2----->0,2
VH2 = 0,2.22,4 = 4,48(l)
\(C_{M\left(ZnSO_4\right)}=\dfrac{0,2}{0,3}=0,667M\)

nCO2=0,075 mol
CO2 + 2KOH => K2CO3 + H2O
0,075 mol =>0,075 mol
CM dd K2CO3=0,075/0,25=0,3M

$2KOH + CO_2 \to K_2CO_3 + H_2O$
$n_{K_2CO_3} = n_{CO_2} = \dfrac{1,68}{22,4} = 0,075(mol)$
$V_{dd} = V_{dd\ KOH} = 0,25(lít)$
$C_{M_{K_2CO_3}} = \dfrac{0,075}{0,25} = 0,3M$
nCO2=0,075(mol)
PTHH: CO2 + 2 KOH -> K2CO3 + H2O
Vddmuoi= VddKOH=0,25(l)
=> nK2CO3=nCO2=0,075(mol)
=>CMddK2CO3=0,075/0,25=0,3(M)

Chọn B
n C O 2 = 0,075 mol
Vì KOH dư nên phản ứng tạo ra muối trung hòa
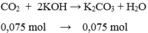
Vì thể tích dung dịch trước và sau không thay đổi


a)
$n_{KOH} = \dfrac{44,8}{56} = 0,8(mol)$
$n_{SO_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
Ta thấy : $n_{KOH} : n_{SO_2} = 0,8 : 0,3 = 2,67 > 2$ nên dung dịch sau phản ứng có : $KOH$ dư ; $K_2SO_3$
b)
$n_{K_2SO_3} = n_{SO_2} = 0,3(mol)$
$\Rightarrow m_{K_2SO_3} = 0,3.158 = 47,4(gam)$
$n_{KOH\ dư} = 0,8 - 0,3.2 = 0,2(mol)$
$\Rightarrow m_{KOH\ dư} = 0,2.56 = 11,2(gam)$

a, Ta có: \(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{KOH}=\dfrac{44,8}{56}=0,8\left(mol\right)\)
\(\Rightarrow\dfrac{n_{KOH}}{n_{SO_2}}=1,3333\)
⇒ Dd sau pư gồm: K2SO3 và KHSO3.
b, PT: \(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
\(SO_2+KOH\rightarrow KHSO_3\)
Giả sử: \(\left\{{}\begin{matrix}n_{K_2SO_3}=x\left(mol\right)\\n_{KHSO_3}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}x+y=0,6\\2x+y=0,8\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{K_2SO_3}=0,2.158=31,6\left(g\right)\\m_{KHSO_3}=0,4.120=48\left(g\right)\end{matrix}\right.\)
Bạn tham khảo nhé!
n SO2 = 4,48/ 22,4 = 0,2 mol
n KOH = 0,3*1 = 0,3 mol
n SO2 < n KOH --> n KOH dư
SO2 + 2KOH --- K2SO3 + H2O
0,2 < 0,3 0,2
CM K2SO4 = 0,2/0,3 = 0,666 M
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right);n_{KOH}=0,3.1=0,3\left(mol\right)\)
Ta có: \(T=\dfrac{n_{KOH}}{n_{SO_2}}=\dfrac{0,3}{0,2}=1,5\) ⇒ tạo ra muối K2SO3 và KHSO3
PTHH: SO2 + 2KOH → K2SO3 + H2O
Mol: x 2x x
PTHH: SO2 + KOH → KHSO3
Mol: y 2y y
Ta có: \(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(C_{M_{ddK_2SO_3}}=\dfrac{0,1}{0,3}=0,333M\)
\(C_{M_{ddKHSO_3}}=\dfrac{0,1}{0,3}=0,333M\)