Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta thấy khi cho Br 2 vào dung dịch 2 muối S 4 + thì toàn bộ S 4 + sẽ bị oxi hoá lên S 6 + ( SO 4 2 - )do đó :
n SO 2 = n SO 4 2 - = 0,15
=> m BaSO 4 = 0,15.233 = 34,95g

$n_{SO_2}=\dfrac{2,24}{22,4}=0,1(mol)$
Quy hỗn hợp về $Fe:x(mol),O:y(mol)$
$\to 56x+16y=30,4(1)$
Bảo toàn e: $3n_{Fe}=2n_O+2n_{SO_2}$
$\to 3x=2y+0,2(2)$
Từ $(1)(2)\to x=0,4(mol);y=0,5(mol)$
Bảo toàn Fe: $n_{Fe_2(SO_4)_3}=0,5x=0,2(mol)$
$\to m_X=0,2.400=80(g)$

Câu 1:
PTHH: \(Na+\dfrac{1}{2}Cl_2\xrightarrow[]{t^o}NaCl\)
Ta có: \(n_{NaCl}=2n_{Cl_2}=2\cdot\dfrac{2,24}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,2\cdot58,5=11,7\left(g\right)\)
Câu 2:
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\) \(\Rightarrow m_{H_2}=0,04\cdot2=0,08\left(g\right)\)
Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\) \(\Rightarrow m_{HCl}=0,08\cdot36,5=2,92\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl}-m_{H_2}=4,29\left(g\right)\)

\(n_{SO_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
0,04<----------------0,02<------0,06
=> mFe = 0,04.56 =2,24 (g)
mFe2(SO4)3 = 0,02.400 = 8 (g)

\(n_{H_2S}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(n_{NaOH}=0.3\cdot0.5=0.15\left(mol\right)\)
\(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0.15}{0.1}=1.5\)
\(\rightarrow\text{Phản ứng tạo ra 2 muối}\)
\(n_{Na_2S}=a\left(mol\right),n_{NaHS}=b\left(mol\right)\)
\(\left\{{}\begin{matrix}2a+b=0.15\\a+b=0.1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.05\\b=0.05\end{matrix}\right.\)
\(m_{\text{Muối}}=0.05\cdot78+0.05\cdot56=6.7\left(g\right)\)

nSO2 = 3,36/22,4 = 0,15 mol; nNaOH = 0,1 mol.
nOH/nSO2 = 2/3 < 1 ---> chỉ có muối axit.
SO2 + NaOH ----> NaHSO3

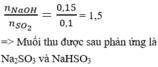
\(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,1---->0,1
=> mNa2S = 0,1.78 = 7,8 (g)