Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/ PTHH chữ: canxi cacbonat =(nhiệt)==> cacbon oxit + cacbonic
PTHH kí hiệu: CaCO3 =(nhiệt)==> CaO + CO2
b/ Áp dụng định luật bảo toàn khối lượng
=> mCaCO3 = mCaO + mCO2 = 56 + 44 = 100 gam
Vì đá vôi chứa 80% CaCO3(nguyên chất)
=> mđá vôi(cần dùng) = \(\frac{100.100}{80}=125gam=0,125kg\)
a) Ta có phương trình hóa học :
Đá vôi -----> CaO + CO2
b) Theo định luật bảo toàn khối lượng
=> mĐá vôi = mCaO + mCO2
=> mĐá vôi = 56 + 44 = 100 (g) hay 0,1 kg
Do trong đá vôi có 80% Canxi cacbonat và 1 số hợp chất không bị phân hủy
=> Khối lượng canxi cacbonat tham gia phản ứng là :
100 * 80% = 80 (g) hay 0,08 kg

PTHH: CaCO3 →to→CaO +CO2
+nCaO=nCO2=0,9(mol)
+mCaO=0,9.56=50,4(gam)
Hiệu suất pư là : \(\dfrac{50,4}{100}=0,504\)

mCaCO3(nguyên chất) = 1 x 90% = 0,9 tấn
PTHH:
CaCO3 ==(nhiệt)==> CaO + CO2
1mol.............................1mol
100 tấn...........................56 tấn
0,9 tấn........................ ......x tấn
=> mCaO(theo phương trình) = \(\frac{0,9.56}{100}=0,504\) tấn
Mà thực tế thu được 0,45 tấn
=> H = \(\frac{0,45}{0,504}.100\%=89,3\%\)
CaCO3(562507)→CaO(562507)+CO2CaCO3(562507)→CaO(562507)+CO2
mCaCO3=1000000.90%=900000(g)mCaCO3=1000000.90%=900000(g)
nCaO=45000056=562507nCaO=45000056=562507
⇒mCaCO3(pứ)=562507.100=56250007(g)⇒mCaCO3(pứ)=562507.100=56250007(g)
⇒H=56250007900000.100%=89,29%

1)
1,2 tấn = 1200(kg)
5 tạ = 500(kg)
mCaCO3=1200.80%=960(kg)mCaCO3=1200.80%=960(kg)
CaCO3to→CaO+CO2nCaCO3 pư=nCaO=50056(mol)⇒H=50056.100960.100%=93%
\(m_{\text{CaCO_3}}=1000.95\%=950kg\\ \rightarrow n_{\text{CaCO_3}}=9,5mol\)
\(m_{CaCO_3}\underrightarrow{t^o}CaO+CO_2\)
9,5 → 9,5
\(\rightarrow V_{CO_2}=9,5.22,4=212,8\)
→ hiệu suất phản ứng là
\(\dfrac{159,6}{212,8}.100=75\%\)

$m_{CaCO_3} = 2500.80\% = 2000(gam)$
$n_{CaCO_3} = \dfrac{2000}{100}= 20(mol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$n_{CaO} = n_{CaCO_3\ pư} = 20.85\% = 17(mol)$
$m_{CaO} = 17.56 = 952(gam)$
\(n_{CaCO_3}=\dfrac{2500.80\%}{100}=20\left(mol\right)\\ PTHH:CaCO_3\underrightarrow{to}CaO+H_2O\\ 20...........20.......20\left(mol\right)\\ n_{CaO\left(TT\right)}=20.85\%=17\left(mol\right)\\ \rightarrow m_{CaO\left(TT\right)}=56.17=952\left(g\right)\)

a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) mCaCO3 = 280 + 110 = 390 kg
=> %CaCO3
= \(\frac{390}{560}\) = 69,7%

a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
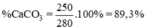

Đá vôi có tên khoa học là Cacbonat canxi với công thức hóa học CaCO3.
Còn vôi sống ký hiệu hóa học là CaO
Tan kiuf nhoa bẹn