Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo đề bài, ta có PTHH:
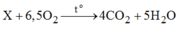
Theo định luật bảo toàn khôi lượng: thì ta có:
1mol chất X phải có 4 mol C ( 4 mol C O 2 ), 10 mol H (5mol H 2 O ) và không chứa oxi ( vì 2 vế của PTHH sô mol nguyên tử oxi bằng nhau). Vậy công thức hóa học của phân tử X là C 4 H 10

Câu 2 :
a)
\(n_{CO_2} = \dfrac{0,3.10^{23}}{6.10^{23}} = 0,05(mol)\\ n_{O_2} = \dfrac{0,9.10^{23}}{6.10^{23}} = 0,15(mol)\)
Vậy :
\(\%n_{CO_2} = \dfrac{0,05}{0,15+0,05}.100\% = 25\%\\ \%n_{O_2} = 100\% - 25\% = 75\%\)
b)
Sục hỗn hợp vào dung dịch Ca(OH)2 lấy dư,thu lấy khí thoát ra ta được O2.Lọc dung dịch,thu lấy kết tủa
\(Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O\)
Cho kết tủa vào dung dịch HCl lấy dư, thu lấy khí thoát ra. Ta thu được khí CO2
\(CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O\)

$n_P = \dfrac{1}{31}(mol)$
$n_{O_2} = \dfrac{1,29}{32} \Rightarrow n_O = 2n_{O_2} = \dfrac{2,58}{32}(mol)$
Suy ra :
$n_P : n_O = \dfrac{1}{31} : \dfrac{2,58}{32} = 2 :5$
Vậy A là $P_2O_5$
hóa trị của P : hóa tri V

\(n_C=n_{CO_2}=\dfrac{8.8}{44}=0.2\left(mol\right)\)
\(n_H=2n_{H_2O}=2\cdot\dfrac{7.2}{18}=0.8\left(mol\right)\)
\(m_O=3.2-0.2\cdot12-0.8=0\)
X chứa : C và H
\(CT:C_xH_y\)
\(x:y=0.2:0.8=1:4\)
\(CTPT:CH_4\)
\(m_{O_2} = 8,8 + 7,2 -3,2 = 12,8(gam) \Rightarrow n_{O_2} = \dfrac{12,8}{32} = 0,4(mol)\\ n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol) ; n_{H_2O} = \dfrac{7,2}{18} = 0,4(mol)\\ \Rightarrow n_{O(trong\ X)} = 0,2.2 + 0,4 - 0,4.2 = 0\)
Vậy X gồm hai nguyên tố : Cacbon và Hidro
\(n_C = n_{CO_2} = 0,2(mol)\\ n_H = 2n_{H_2O} = 0,4.2 = 0,8(mol)\\ n_C : n_H = 0,2 : 0,8 = 1 : 4\)
X là CH4
