Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
![]()
Vì mdd tăng = m C O 2 + m H 2 O - m C a C O 3
⇒ m C O 2 + m H 2 O = 35 , 4 ( g )
Dễ thấy trong dung dịch sau phản ứng còn Ca(HCO3)2 vì nếu Ca(OH)2 dư như các bài trước ta đã gặp thì khối lượng dung dịch phải giảm chứ không tăng.
Bảo toàn Ca:
n C a ( H C O 3 ) 2 = 0 , 25 ( m o l ) .
Bảo toàn C:
n C O 2 = 2 n C a ( H C O 3 ) 2 + n C a C O 3 = 0 , 6 ( m o l )
⇒ n H 2 O = 0 , 5 ( m o l )
Vì các axit đồng đẳng với axit acrylic nên sẽ có công thức chung là CnH2n-2O2
![]()
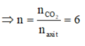
Vậy m a x i t = m C 6 H 10 O 2 = 11 , 4 ( g )
![]()
![]()

Đáp án C
MY = 16,7 => chứng tỏ H2 dư
Y gồm C3H8 và H2 ; nY = 0,01 mol
=> nC3H8 = 0,0035 ; nH2 = 0,0065 mol
nCa(OH)2 = 0,006 mol => nOH = 0,012 mol
Đốt cháy X thì tạo sản phẩm với lượng giống như đốt cháy Y
=> nCO2 = 3nC3H8 = 0,0105 mol ; nH2O = 0,0205 mol
=> nCaCO3 = nOH – nCO2 = 0,0015 mol
=> mCaCO3 – (mCO2 + mH2O) = - 0,681g
=> m dung dịch tăng 0,681g

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron

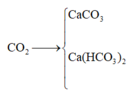
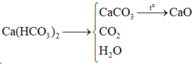
=> nCO2 = nCaCO3 + 2nCaO = 20/100 + 2.5,6/56 = 0,4
X gồm C4H8O2, C4H12N2 =>nX = 0,4/4 = 0,1
=> mX = 0,1.88 = 8,8g => Chọn C.

quy đổi hh thành fe,cu,s : 56x+64y+32z=6,48 (1)
Fe--->fe+3+3e
cu--->cu+2+2e
s--->s+4+4e
o2+4e---->2o2-
bte:3x+2y+0,28=0,45 (2)
giải 12--->x=0,03 ,y=0,04
phần :2 fe--->fe+3+3e
cu---->cu+2+2e
n+5+1e--->
s--->s+6
<=>0,03.3+0,04.2+0,07.6=nNO2====>v=13,216 l
ket tủa có :Fe(oH)3=nFe;cu(oh)2=nCu;BaSO4=nS--->m=23,44g
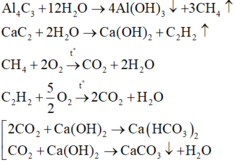

Chọn A
75