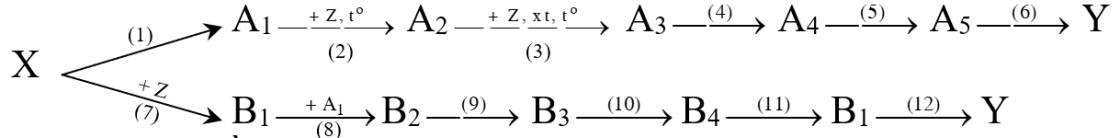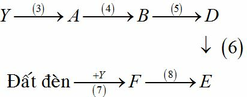Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

%Na = 39,316% => MZ = 58,5
=> Z là NaCl
=> X là H2 và Y là HCl
Pt: Cl2 + H2 → 2HCl
HCl + NaOH → NaCl + H2O
2NaCl + H2SO4đặc → Na2SO4 + 2HCl
4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O

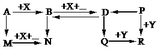
– Xác định các chất:
A là NaOH; B là Na2CO3; D là NaHCO3; M là NaAlO2; N là Al(OH)3;
P là Ba(HCO3)2; R là BaSO4; Q là BaCO3; Y là NaHSO4; X là CO2
– Các phương trình phản ứng:
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + CO2 + H2O →2NaHCO3
2NaHCO3 →Na2CO3 + CO2 + H2O
NaOH + Al + H2O → NaAlO2 + 3/2H2
NaAlO2 + CO2 + 2H2O → NaHCO3 + Al(OH)3
3Na2CO3 + 2AlCl3 + 3H2O →6NaCl + 3CO2 + Al(OH)3
2NaHCO3 + Ba(OH)2 → Na2CO3 + BaCO3 + 2H2O
BaCO3 + 2NaHSO4 →BaSO4 + CO2 + Na2SO4 + H2O
Ba(HCO3)2 + 2NaHSO4 →BaSO4 + 2CO2 + Na2SO4 + 2H2O
Ba(HCO3)2 + Na2SO4 →BaSO4 + 2NaHCO3

a) X là Cl2
Z là hợp chất 2 nguyên tố, Z là muối của Kali trong đó chiếm 52,35% về khối lượng => Z là KCl
Y là hợp chất 2 nguyên tố, trong đó có chứa Clo, dd Y làm quỳ tím chuyển sang màu đỏ => Y là axit => Y là HCl
Đất đèn +HCl → F => F là C2H2
Ta có sơ đồ sau:
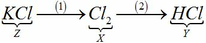

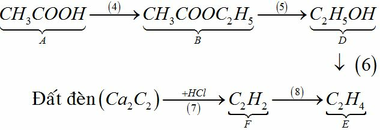
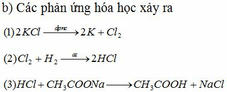
4 C H 3 C O O N a + C 2 H 5 O H ↔ H 2 S O 4 , t ∘ C H 3 C O O C 2 H 5 + H 2 O 5 C H 3 C O O C 2 H 5 + N a O H → C H 3 C O O N a + C 2 H 5 O H
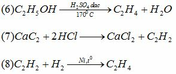

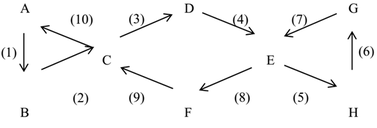
PTHH:
2Al+6HCl→2AlCl3+3H2
Fe+2HCl→FeCl2+H2
2NaOH+FeCl2→2NaCl+Fe(OH)2
3NaOH+AlCl3→3NaCl+Al(OH)3
NaOH+Al(OH)3→NaAlO2+2H2O
4Fe(OH)2+O2→2Fe2O3+4H2O
CO2+NaAlO2+2H2O→Al(OH)3+NaHCO3


a)Theo đề bài ta có :
mct=mH2SO4=\(\dfrac{100.20}{100.98}\approx0,204\left(mol\right)\)
nCuO=\(\dfrac{1,6}{80}=0,02\left(mol\right)\)
PTHH :
CuO + H2SO4 \(\rightarrow\) CuSO4 + H2O
0,02mol...0,02mol...0,02mol
Theo pthh ta có tỉ lệ :
nCuO=\(\dfrac{0,02}{1}mol< nH2SO4=\dfrac{0,204}{1}mol\)
=> số mol của H2SO4 dư ( tính theo số mol của CuO)
b) Các chất có trong dung dịch sau p/ư gồm CuSO4 và H2SO4 dư
Ta có
mct=mCuSO4=0,02.160=3,2 g
mct=mH2SO4(dư) = (0,204-0,02).98=18,032 g
mddCuSO4= 1,6 + 100 = 101,6 (g)
=> C%\(_{C\text{uS}O4}=\dfrac{mct}{m\text{dd}}.100\%=\dfrac{3,2}{101,6}.100\%\approx3,15\%\)\(\)
C%\(_{H2SO4\left(d\text{ư}\right)}=\dfrac{mct}{m\text{dd}}.100\%=\dfrac{18,032}{101,6}.100\%\approx17,75\%\)
- Khối lượng axit sunfuric: \(\dfrac{20.100}{100}\) = 20g
a, Phương trình phản ứng:
\(CuO+H_2SO_4-->CuSO_4+H_2O\)
b, Tính nồng độ phần trăm các chất:
\(CuO+H_2SO_4-->CuSO_4+H_2O\)
80g........................98g
1,6g............................20g
-H2SO4 dư, tính theo CuO:
\(CuO+H_2SO_4-->CuSO_4+H_2O\)
80g........................ 98g 160g
1,6g......................... ?...................?
\(m_{H_2SO_4}\left(phan.ứng\right)=\dfrac{1,6.98}{80}=1,96g\)
\(m_{H_2SO_4}\left(sau.phan.ung\right)=20-1,96=18,04g\)
- Khối lượng dung dịch sau PƯ:
m dd = m CuO + m dd axit = 1,6 + 100 = 101,6g
\(\%m_{H_2SO_4}=\dfrac{18,04}{101,6}.100\approx17,75\%\)
\(m_{CuSO_4}=\dfrac{1,6.160}{80}=3,2g\)
\(\%m_{H_2SO_4}=\dfrac{3,2}{101,6}.100\approx3,15\%\)
Vậy..........................

a)
Dung dịch X gồm $Ca(OH)_2,Ba(OH)_2$ làm đổi màu quỳ tím chuyển màu xanh.
b)
$Ca + 2H_2O \to Ca(OH)_2 + H_2$
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
Gọi $n_{Ca} = a ; n_{Ba} = b$
Ta có :
$m_{hh} = 40a + 137b = 17,7(gam)$
$n_{H_2} = a + b = 0,2(mol)$
Suy ra a = b = 0,1
$\%m_{Ca} = \dfrac{0,1.40}{17,7}.100\% = 22,6\%$
$\%m_{Ba} = 100\%-22,6\% = 77,4\%$
c)
$n_{Ca(OH)_2} = n_{Ba(OH)_2} = a = b = 0,1(mol)$
$m_{Ca(OH)_2} = 0,1.74 = 7,4(gam)$
$m_{Ba(OH)_2} = 0,1.171 = 17,1(gam)$