Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án:
8,625 g
Giải thích các bước giải:
nCl2=22,4/22,4=1 mol
nNaOH=0,1x2=0,2 mol
nCa(OH)2=0,1x0,5=0,05 mol
2NaOH+Cl2->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2+2Cl2->CaCl2+Ca(ClO)2+2H2O
0,05 0,05 0,025
m=0,025x111+0,1x58,5=8,625 g

Gọi chung Cl2 và Br2 là X2, 2 bazo là ROH
X2 + 3ROH → 2RX + RXO3 + 3H2O
X2 + 2ROH→ RX + RXO + H2O
nROH = 0.5 mol
nX2 = 0.25 mol
→ Phản ứng xảy ra là phản ứng 2 (nROH = 2nX2)
Cl2 phản ứng trước Br2
X2 + 2ROH→ RX + RXO + H2O
→ Cl2 + 2ROH → NaCl + NaClO + H2O
----0.1-----0.2--------0.1
mH2O = 0.1 x 18 = 1.8g
nROH = 0,5 → mROH = 24.8g (0.2 NaOH, 0.3 KOH)
→ nROH = 0,2 → mROH = 9.92g
[m] mRCl = mCl2 + mROH p/ứ - mH2O
= 7.1 + 9.92 - 1.8 = 15,22.
1.
nCl2 = \(\frac{0,896}{22,4}\) = 0,04 (mol) , nNaOH = 1.0,2 = 0,2 (mol)
............Cl2 + 2NaOH → NaCl + NaClO + H2
Đầu.. 0,04........0,2
Pư .......0,04.......0,08............0,04.........0,04.........0,04
Spư......0............0,16............0,04.........0,04.........0,04
CM NaCl = \(\frac{0,04}{0,2}=0,2M\)
CM NaClO = CM NaCl = 0,2 M
CM NaOH = \(\frac{0,12}{0,2}=0,6M\)

\(a.2Fe+6H_2SO_{4\left(đặc\right)}\rightarrow\left(t^o\right)Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\\ n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ n_{Fe}=\dfrac{2}{3}.0,15=0,1\left(mol\right)\\ n_{Fe_2\left(SO_4\right)_3}=\dfrac{0,15}{3}=0,05\left(mol\right)\\ a,m=m_{Fe}=0,1.56=5,6\left(g\right)\\ b,m_{Fe_2\left(SO_4\right)_3}=400.0,05=20\left(g\right)\)

Bài 1:
Giả sử 2 muối NaX và NaY đều cho kết tủa:
Ta có
\(NaM+AgNO_3\rightarrow AgX+NaNO_3\)
\(m_{tang}=\left(108-23\right).nM=8,61-6,03\)
\(\rightarrow n_M=0,03\left(mol\right)\)
\(M_M=\frac{6,03}{0,03-23}=175,6\)
Không có một halogen nào thỏa mãn.
Phải có một muối là NaF (AgF không kết tủa), vì là 2 halogen thuộc 2 chu kì liên tiếp nên Y là Cl
\(n_{AgCl}=\frac{8,61}{143,5}=0,06\left(mol\right)\)
\(\rightarrow n_{NaCl}=0,06\left(mol\right)\)
\(\rightarrow m_{NaF}=6,03-0,06.58,5=2,52\left(g\right)\)
\(\%m_{NaF}=\frac{2,52}{6,03}.100\%=41,79\%\)
Bài 2:
Spu, \(m_{giam}=m_{Br^-}-m_{Cl}=1,6-1,155=0,445\left(mol\right)\)
Gọi x là mCl- thì x+0,445 là mBr-
\(Cl_2+2Br^-\rightarrow Br_2+2Cl^-\)
\(\rightarrow n_{Cl^-}=n_{Br^-}\)
\(\Leftrightarrow\frac{x}{35,5}=\frac{x+0,445}{80}\)
\(\rightarrow35,5.\left(x+0,445\right)=80x\)
\(\Leftrightarrow x=0,355\)
\(n_{Cl^-}=\frac{0,335}{35,5}\left(mol\right)\)
\(\rightarrow n_{Cl2}=\frac{0,335}{71}\left(mol\right)\)
\(\rightarrow m_{Cl2}=0,335\left(g\right)\)
\(\%_{Cl2}=\frac{0,335.100}{5}=6,7\%\)
Bài 4:
Chất ko tan là Cu
\(\rightarrow m_{Mg,Al}=10,14-6,4=3,74\left(g\right)\)
\(n_{H2}=0,35\left(mol\right)\)
\(\rightarrow n_{HCl}=2n_{H2}=0,7\left(mol\right)=n_{Cl}\)
\(\rightarrow m_{Cl}=24,85\left(g\right)\)
\(m_{muoi}=3,75+24,85=29,59\left(g\right)\)

1,\(n_{hhB}=\frac{11,2}{22,4}=0,5\left(mol\right)\)
\(d_{\frac{hhB}{H_2}}=\frac{\overline{M}}{2}=8\Rightarrow\overline{M}=16\)
ta có sơ đồ dường chéo:
H 2 NO = 2 30 16 14 14
=>\(\frac{n_{H_2}}{n_{NO}}=1\Rightarrow n_{H_2}=n_{NO}=0,25\left(mol\right)\)
ta có các quá trình nhường nhận e:
\(Mg^0\rightarrow Mg^{+2}+2e\) \(Al^0\rightarrow Al^{+3}+3e\)
\(N^{+5}+3e\rightarrow N^{+2}\) \(2H^{+1}+2e\rightarrow H_2^0\)
0,25................0,25 0,25
mNO3=0,25.62=15,5(g)
mSO4=0,25.96=24(g)
=>mmuối=mkl+mNO3+mSO4=8,5+15,5+24=48(g)

0,44-->0,22n--> 0,22
theo bài ra ta có :
0,22( 23 . 2 +nB) = 45,32
nB=160
+ với n=1 => B=160(loại)
+ n=2 => B = 80 (B là brom)
gọi số khối của đồng vị thứ nhất là B =>số khối của đồng vị thứ hai là B+2
theo bài ra ta có pt:
Số khối của đồng vị thứ hai là: 80
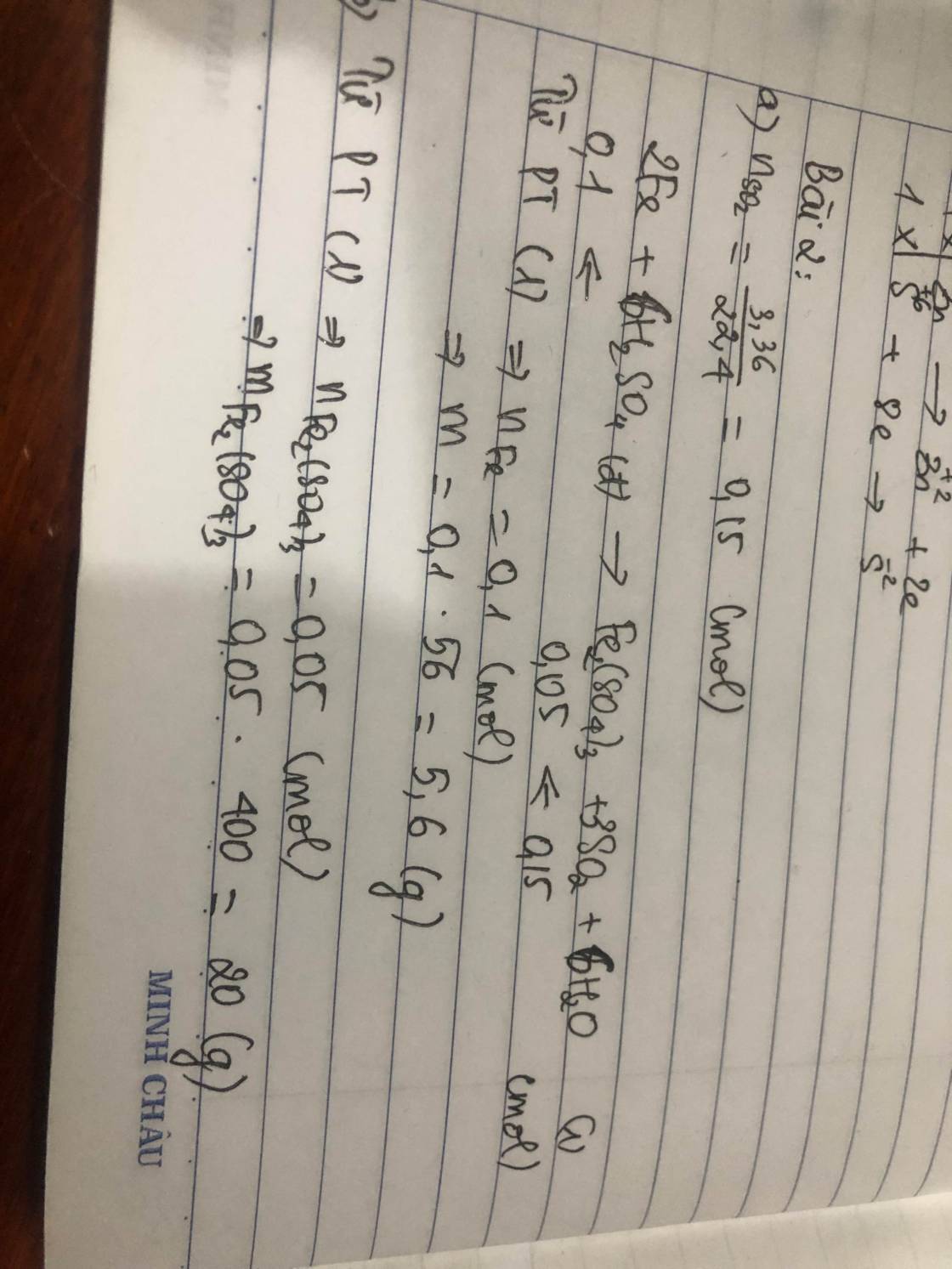
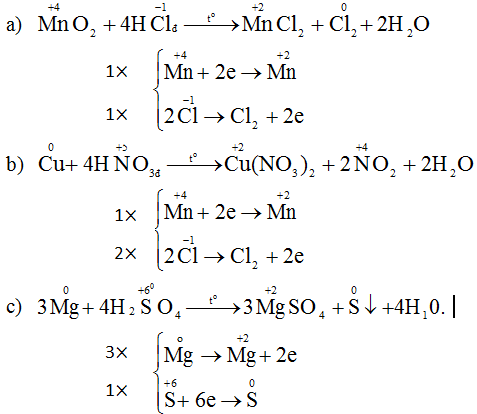
Đáp án C