Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

giả sử kết tủa chỉ có BaSO4 => mBaSO4 =0,15 .233 =34,95 < 49,725 => kết tủa gồm BaCO3 và BaSO4
giả sử trong dd X chỉ có muối CO3 2- => nH+ = 0,3 .2 =0,6 > 0,525 => loại
trong dd X chỉ có HCO3- => nH+ = 0,3 => loại
vậy trong X có cả 2 muối trên
mBaCO3 =m kết tủa - mBaSO4 => nBaCO3 = 0,075
nCO2 =0,075 + 0,3 =0,375 => V=8,4

Bài 1:
\(n_{NaOH}=0,25.2=0,5\left(mol\right)\\ n_{AlCl_3}=0,25x\left(mol\right)\\ 3NaOH+AlCl_3\rightarrow Al\left(OH\right)_3+3NaCl\left(1\right)\\ Al\left(OH\right)_3+NaOH\left(dư\right)\rightarrow NaAlO_2+2H_2O\left(2\right)\\ n_{Al\left(OH\right)_3\left(còn\right)}=\dfrac{7,8}{78}=0,1\left(mol\right)\\Đặt:n_{NaOH\left(1\right)}=a\left(mol\right);n_{NaOH\left(2\right)}=b\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,5\\b-\dfrac{1}{3}a=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,2\end{matrix}\right.\\ \Rightarrow n_{AlCl_3}=\dfrac{0,3}{3}=0,1\left(mol\right)\\ \Rightarrow x=C_{MddAlCl_3}=\dfrac{0,1}{0,25}=0,4\left(M\right)\)
Bài 2:
\(n_{AlCl_3}=\dfrac{26,7}{133,5}=0,2\left(mol\right)\\ 3NaOH+AlCl_3\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\left(1\right)\\ Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\left(2\right)\\ n_{Al\left(OH\right)_3\left(còn\right)}=\dfrac{11,7}{117}=0,1\left(mol\right)\\ Đặt:n_{NaOH\left(1\right)}=a\left(mol\right);n_{NaOH\left(2\right)}=b\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}\dfrac{1}{3}a=0,2\\\dfrac{1}{3}a-b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,6\\b=0,1\end{matrix}\right.\Rightarrow V=V_{ddNaOH}=\dfrac{0,6+0,1}{1}=0,7\left(l\right)\)

Tổng cộng nhiệt lượng khi đun 1 lít nước này là: 33,6+33,6*10:100=39,96g
Do đó 2 lít cần:39,96*2=79,92g
nCH4=890:79,92*1/890=25/1998 mol
nbiogas=25/1998:60*100=125/5994 mol
Vbiogas=125/5994*22,4=1408/2997~0,467 lít

a)
Cho Zn :
- Viên kẽm tan dần , sủi bọt khí không màu
Cho ZnO :
- Chất rắn tan dần
Cho Al2O3
- Chất rắn tan dần
\(2NaOH+Zn+2H_2O\rightarrow Na_2ZnO_2+2H_2\)
\(2NaOH+ZnO\rightarrow Na_2ZnO_2+H_2O\)
\(2NaOH+Al_2O_3\rightarrow2NaAlO_2+H_2O\)
b) Ban đầu không có hiện tượng gì. Sau một thời gian, dung dịch chuyển dần sang màu hồng. Sau đó mất màu ngay lập tức.
\(NaOH+HCl\rightarrow NaCl+H_2O\)

Chọn B
Phản ứng khử oxit của CO có thể hiểu là:
![]()
Trước là 44,8 g oxit sau thu được 40g chất rắn.
Vậy lượng chất rắn sau phản ứng bị giảm.
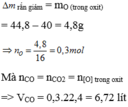

a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(n_{HCl}=\dfrac{150}{1000}.2=0,3\left(mol\right)\)
Ta thấy: \(\dfrac{0,05}{1}< \dfrac{0,3}{2}\)
Vậy HCl dư.
Vậy trong X chứa FeCl2 và HCl dư.
b. PTHH:
2NaOH + FeCl2 ---> Fe(OH)2 + 2NaCl (2)
HCl + NaOH ---> NaCl + H2O (3)
Theo PT(1): \(n_{H_2}=n_{Fe}=0,05\left(mol\right)\)
=> \(V_{H_2}=0,05.22,4=1,12\left(lít\right)\)
c. Theo PT(1): \(n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\)
Theo PT(2): \(n_{Fe\left(OH\right)_2}=n_{FeCl_2}=0,05\left(mol\right)\)
=> \(m_{Fe\left(OH\right)_2}=0,05.90=4,5\left(g\right)\)

a/ \(C_2H_2\left(0,15\right)+2Br_2\left(0,3\right)\rightarrow C_2H_2Br_4\left(0,15\right)\)
\(n_{C_2H_2Br_4}=\dfrac{51,9}{346}=0,15\left(mol\right)\)
\(\Rightarrow m_{C_2H_2}=0,15.26=3,9\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%C_2H_2=\dfrac{3,9}{10}.100\%=39\%\\\%C_2H_6=100\%-39\%=61\%\end{matrix}\right.\)
b/ \(m_{C_2H_6}=10-3,9=6,1\left(g\right)\)
\(\Rightarrow n_{C_2H_6}=\dfrac{6,1}{30}=\dfrac{61}{300}\left(mol\right)\)
\(\Rightarrow V_{C_2H_6}=\dfrac{61}{300}.22,4=4,56\left(l\right)\)
c/ \(m_{Br_2}=0,3.160=48\left(g\right)\)
\(\Rightarrow m_{ddBr_2}=\dfrac{48}{16\%}=300\left(g\right)\)

a/ \(n_{CO_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(n_{Ba\left(OH\right)}=0,4.0,1=0,04\)
\(n_{NaOH}=0,2.0,1=0,02\left(mol\right)\)
Vì \(n_{Ba\left(OH\right)_2}>n_{CO_2}\) nên chỉ xảy ra phản ứng.
\(Ba\left(OH\right)_2+CO_2\left(0,02\right)\rightarrow BaCO_3\left(0,02\right)+H_2O\)
\(\Rightarrow m_{BaCO_3}=0,02.107=3,94\left(g\right)\)
b/ Khối lượng tối đa kết tủa có thể có là: \(0,04.197=7,88\left(g\right)\)
Vì khối lượng kết tủa thực tế bé hơn khối lượng kết tủa tối đa nên ta chia làm 2 trường hợp.
TH 1: \(Ba\left(OH\right)_2\) dư.
\(Ba\left(OH\right)_2+CO_2\left(0,01\right)\rightarrow BaCO_3\left(0,01\right)+H_2O\)
\(n_{BaCO_3}=\dfrac{1,97}{197}=0,01\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,01.22,4=0,224\left(l\right)\)
TH 2: \(Ba\left(OH\right)_2\) hết.
\(Ba\left(OH\right)_2\left(0,04\right)+CO_2\left(0,04\right)\rightarrow BaCO_3\left(0,04\right)+H_2O\)
\(2NaOH\left(0,02\right)+CO_2\left(0,01\right)\rightarrow Na_2CO_3\left(0,01\right)+H_2O\)
\(Na_2CO_3\left(0,01\right)+CO_2\left(0,01\right)+H_2O\rightarrow2NaHCO_3\)
\(BaCO_3\left(0,03\right)+CO_2\left(0,03\right)+H_2O\rightarrow Ba\left(HCO_3\right)_2\)
\(\Rightarrow n_{BaCO_3\left(pứ\right)}=0,04-0,01=0,03\left(mol\right)\)
\(\Rightarrow n_{CO_2}=0,04+0,01+0,01+0,03=0,09\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,09.22,4=2,016\left(l\right)\)
c/ Vì khi cho \(HCl\) dư (bắt buộc phải dư hoặc vừa đủ nhé. Chứ không thể như cái đề được đâu) ta thu được\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\) nên ta chia thành các trường hợp sau.
TH 1: \(A=\left\{{}\begin{matrix}Na_2CO_3\\NaOH\end{matrix}\right.\)
\(Na_2CO_3\left(0,04\right)+2HCl\rightarrow2NaCl+H_2O+CO_2\left(0,04\right)\)
\(\Rightarrow n_{NaOH}=2.n_{Na_2CO_3}=2.0,04=0,08>0,02\left(l\right)\)
TH 2: \(A=\left\{{}\begin{matrix}Na_2CO_3:x\left(mol\right)\\NaHCO_3:y\left(mol\right)\end{matrix}\right.\)
Dễ dàng suy ra được hệ:
\(\left\{{}\begin{matrix}2x+y=0,02\\x+y=0,08\end{matrix}\right.\)(loại vì không có nghiêm dương)
TH 3: \(A=\left\{{}\begin{matrix}NaHCO_3:0,02\left(mol\right)\\Ba\left(HCO_3\right)_2:z\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow0,02+2z=0,08\)
\(\Leftrightarrow z=0,03\left(mol\right)\)
Từ đây ta có sau khi phản ứng kết thúc thì thu được:
\(\left\{{}\begin{matrix}A:NaHCO_3\left(0,02\right);Ba\left(HCO_3\right)_2\left(0,03\right)\\B:BaCO_3\left(t\right)\end{matrix}\right.\)
\(\Rightarrow t=0,04-0,03=0,01\left(mol\right)\)
\(\Rightarrow m_{BaCO_3}=0,01.197=1,97\left(g\right)\)
Đựa vô câu b ta suy ra được thể tích \(V_{CO_2}=2,016\left(l\right)\)

Ta có: \(n_{K_2CO_3}=\dfrac{13,8}{138}=0,1\left(mol\right)\)
\(PTHH:H_2SO_4+K_2CO_3--->K_2SO_4+H_2O+CO_2\)
Theo PT: \(n_{H_2SO_4}=n_{K_2CO_3}=0,1\left(mol\right)\)
\(\Rightarrow V_{dd_{H_2SO_4}}=\dfrac{0,1}{1}=0,1\left(lít\right)\)