Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Coi như hỗn hợp X chỉ gồm Na, K, Ba, O
Cho X vào nước thì 3 kim loại phản ứng sinh ra khí H2, còn O tác dụng với H2 để tạo ra nước theo tỷ lệ 1Oxi+1H2
\(\Rightarrow\) \(n_{H_2}=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_O=0,14\left(mol\right)\)
Có \(n_{Na}=n_{NaOH}=0,18\left(mol\right)\)
\(n_K=n_{KOH}=\frac{0,044m}{56};n_{Ba}=n_{Ba\left(OH\right)_2}=\frac{0,93m}{171}\left(mol\right)\)
\(\Rightarrow n_O=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_{H_2}=0,09+\frac{0,022m}{56}+\frac{0,465m}{171}\)
Lại có phương trình tổng khối lượng hỗn hợp X:
\(m_X=m=m_{Na}+m_K+m_{Ba}+m_O\\ =0,18.23+\frac{0,044m}{56}.39+\frac{0,93m}{171}.137+m_O\)
Thay số mol Oxi tính được (theo m) ở trên vào ta được phương trình 1 ẩn m
giải ra được \(m\approx25,5\)

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Mình nghĩ bạn chưa hiểu rõ vấn đề ban đầu nó :
H+ +CO3 2- => HCO3-
Sau đó
HCO3 - + H+ => co2
Như vậy bài toán sẽ ra 0,01 mol co2 là đáp án C

tính theo phương trình là ra : 1) CO2 + 2KOH === > K2CO3 + H2O
2) CO2 + KOH ==== > KHCO3
N2 ko phản ứng
Đáp số 28 %

N+5 +1e =>N+4
0,02 mol<=0,02 mol
2N+5 +2.4e =>2N+1
0,04 mol<=0,01 mol
ne nhận=ne nhường=0,06 mol
nNO3- tạo muối=ne nhận=0,06 mol
=>mNO3-=0,06.62=3,72g
mKL=5,04g=>m muối=m gốc KL+mNO3-=3,72+5,04=8,76g
nHNO3 =0,06+0,02+0,005.2=0,09 mol
=>CM dd HNO3=0,09/0,1=0,9M
Phương trình nhận electron:
N+5 + 8e → N2O
N+5 +1e→NO2
nNO tạo muối = nNO + 8nN2O = 0,02 + 8.0,005 = 0.02 + 0,04 = 0,06 mol
mNO tạo muối =0,06.62 = 3,72g
m =mKL+ mNO tạo muối = 5,04 + 3,72 = 8,76g
nHNO3 tham gia phản ứng = 2nNO + 10nN2O = 2.0,02 + 10.0,005= 0,09 mol
x =0.09:0,1=0,9M ==>> Đáp án thứ nhất
 với các chất sau:
với các chất sau:
+ Tính các giá trị đã biết:
+ Với bài toán tổng hợp như này, thì ta phải viết các phương trình cụ thể cho dễ quan sát:
(1) H+ + CO3- ⟶ HCO3-
(2) H+ + HCO3- ⟶ CO2 +H2O.
Vì thu được khí CO2 nên có xảy ra phản ứng (2) ⇒ CO32- đã phản ứng hết với H+.
+ Từ
+ Vì khi thêm dung dịch Ba(OH)2 vào dung dịch Y thu được kết tủa nên trong Y phải có muối HCO3-
Như vậy suy ra ngay HCl đã phản ứng hết
Do đó từ (1) và (2) ta suy ra
Loại ngay các đáp án A và B.
Việc cần thực hiện bây giờ là đi tính nồng độ của KHCO3 trong dung dịch X:
Vậy dung dịch Y chỉ chứa các ion K+, Na+, HCO3- và Cl-.
+ Khi thêm dịch Ba(OH)2 dư vào dung dịch Y thì:
Sau đó thì
+ Do đó 29,55 gam kết tủa là BaCO3:
Ta sử dụng Bảo toàn nguyên tố C, toàn bộ C trong dung dịch Y chuyển hóa hết về trong kết tủa (vì thêm dung dịch Ba(OH)2 dư vào):
+ Lại áp dụng bảo toàn nguyên tốC ta được:
Hay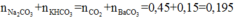
Đáp án D