Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có 2 phản ứng mà H+ đóng vai trò là chất oxi hóa: (a), (d). Đáp án A

`n_{Ba(OH)_2}=0,135.2=0,27(mol)`
`n_{Al_2(SO_4)_3}=0,08.1=0,08(mol)`
`Al_2(SO_4)_3+3Ba(OH)_2->2Al(OH)_3+3BaSO_4`
`0,08->0,24->0,16->0,24(mol)`
`->n_{Ba(OH)_2\ du}=0,27-0,24=0,03(mol)`
`Ba(OH)_2+2Al(OH)_3->Ba(AlO_2)_2+4H_2O`
`0,03->0,06(mol)`
`->n_{Al(OH)_3\ du}=0,16-0,06=0,1(mol)`
`2Al(OH)_3` $\xrightarrow{t^o}$ `Al_2O_3+3H_2O`
`0,1->0,05(mol)`
`->a=m_{Al_2O_3}+m_{BaSO_4}=0,05.102+0,24.233=61,02(g)`

Đáp án A
Các phương trình phản ứng:
Dung dịch H2SO4 20% thuộc loại dung dịch loãng.
Phương trình phản ứng:
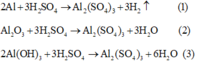
Do các chất tác dụng vừa đủ với nhau
=> dung dịch sau chỉ có chất tan là Al2(SO4)3.
Tính toán:
Ta có: n H 2 = 5 , 04 22 , 4 = 0 , 225 mol
Sơ đồ phản ứng:
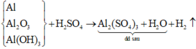
Khối lượng Al2(SO4)3 trong dung dịch sau là:
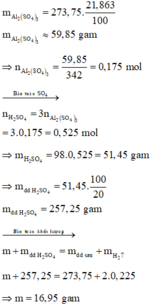

Vì sản phẩm khử của H2SO4 đặc có nhiều dạng như SO2, S, H2S nên bài toán sử dụng cách truyền thống (viết phương trình, cân bằng và đặt ẩn) sẽ không khả thi. Vì vậy sử dụng định luật bảo toàn là cách hợp lí.
Gọi sản phẩm khử là X và k là số electron mà H2SO4 nhận để tạo ra X.
Sơ đồ phản ứng:
Al+H2SO4 đặc->Al2(SO4)3+X+H2O
![]()
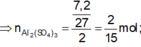
![]()
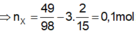


Theo giả thiết ta có: \(n_{Al_2\left(SO_4\right)_3}=0,08\left(mol\right)\)
\(Al_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow2Al\left(OH\right)_3+3BaSO_4\) (1)
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\) (2)
Giả sử kết tủa chỉ là BaSO4 thì nhận thấy \(n_{\downarrow}< n_{SO_4}\). Do đó chỉ xảy ra phản ứng (1).
Gọi số mol Ba(OH)2 là x (mol)
Bảo toàn nguyên tố ta có: \(n_{BaSO_4}=x\left(mol\right);n_{Al\left(OH\right)_3}=\dfrac{2x}{3}\left(mol\right)\)
\(\Rightarrow233x+78.\dfrac{2x}{3}=51,3\Rightarrow x=0,18\)
\(\Rightarrow V=\dfrac{0,18}{2}=0,09\left(l\right)\)

\(n_{Al2\left(SO4\right)3}=0,1.1=0,1\left(mol\right)\)
Pt : \(2K+2H_2O\rightarrow2KOH+H_2\)
0,3 0,3
\(6KOH+Al_2\left(SO_4\right)_3\rightarrow3K_2SO_4+2Al\left(OH\right)_3\)
0,3 0,1 0,15 0,1
a) A : khí H2 , D : Kết tủa Al(OH)3
b) Xét tỉ lệ : \(\dfrac{0,3}{6}< \dfrac{0,1}{1}=>Al_2\left(SO_4\right)_3dư\)
\(\Rightarrow m_D=m_{Al\left(OH\right)3}=0,1.78=7,8\left(g\right)\)
c) Dung dịch D gồm : Al2(SO4)3 dư và K2SO4
\(C_{MK2SO4}=\dfrac{0,15}{0,1}=1,5\left(M\right)\)
\(C_{MAl2\left(SO4\right)3dư}=\dfrac{0,1-\dfrac{0,3}{6}}{0,1}=0,5\left(M\right)\)
Chúc bạn học tốt

1 gam H2 ⇒ nH2 = $\frac{1}{2}$mol
3 mol H2 : ${\Delta _r},H_{298}^0$ = 250 kJ.
$\frac{1}{2}$ mol H2 : ${\Delta _r},H_{298}^0$ = 250. $\frac{1}{2}$ :3 = 41,67 kJ.
⇒ Để thu được 1 gam H2, phản ứng này cần hấp thu 41,67 kJ.
\(n_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 _______________ 0,1____________
\(\rightarrow m_{Al2\left(SO4\right)3}=0,1.342=34,2\left(g\right)\)