Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Mg + 2HCl -> MgCl2 + H2 (1)
nMg=0,05(mol)
nHCl=0,3(mol)
Vì 0,05.2<0,3 nên sau PƯ còn HCl dư
Từ 1:
nMg=nMgCl2=nH2=0,05(mol)
mMgCl2=95.0,05=4,75(g)
VH2=22,4.0,05=1,12(lít)

Bài 6:
\(a.n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\\ n_{Mg}=\dfrac{14,4}{24}=0,6\left(mol\right)\\ PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ Vì:\dfrac{0,2}{1}< \dfrac{0,6}{2}\\ \rightarrow Mgdư\\ n_{H_2}=n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ b.m_{MgCl_2}=0,2.95=19\left(g\right)\)
c. Số phân tử chất còn dư sau phản ứng là 0. Vì chất dư sau phản ứng là nguyên tử Mg.
Bài 7:
\(a.n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\\ n_{HCl}=\dfrac{43,8}{36,5}=1,2\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Vì:\dfrac{0,3}{2}< \dfrac{1,2}{6}\\ \rightarrow HCldư\\ n_{H_2}=\dfrac{3}{2}.0,3=0,45\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,45.22,4=10,08\left(l\right)\\ b.n_{AlCl_3}=n_{Al}=0,3\left(mol\right)\\ \rightarrow m_{AlCl_3}=0,3.133,5=40,05\left(g\right)\)
c. Số phân tử chất còn dư sau phản ứng là số phân tử HCl còn dư và bằng:
\(\left(1,2-\dfrac{6}{2}.0,3\right).6.10^{23}=1,8.10^{23}\left(phân.tử\right)\)

Bài 7 :
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{43,8}{36,5}=1,2\left(mol\right)\)
Pt : 2Al + 6HCl → 2AlCl3 + 3H2\(|\)
2 6 2 3
0,3 1,2 0,3 0,45
a) Lập tỉ số so sánh : \(\dfrac{0,3}{2}< \dfrac{1,2}{6}\)
⇒ Al phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Al
Số mol của khí hidro
nH2 = \(\dfrac{0,3.3}{2}=0,45\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,45 . 22,4
= 10,08 (g)
b) Số mol của nhôm clorua
nAlCl3 = \(\dfrac{0,45.2}{3}=0,3\left(mol\right)\)
Khối lượng của nhôm clorua
mAlCl3 = nAlCl3 . MAlCl3
= 0,3. 133,5
= 40,05 (g)
c) Số mol dư của axit clohidric
ndư = nban đầu - nmol
= 1,2 - (\(\dfrac{0,3.6}{2}\))
= 0,3 (mol)
⇒ A = 0,3 . 6. 10-23 = 1,8 .10-23 (phân tử)
Chúc bạn học tốt
Bài 8 :
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Số mol của khí oxi ở dktc
nO2 = \(\dfrac{V_{O2}}{22,4}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Pt : 4Al + 3O2 → (to) 2Al2O3\(|\)
4 3 2
0,2 0,6 0,1
a) Lập tỉ số so sánh : \(\dfrac{0,2}{4}< \dfrac{0,6}{3}\)
⇒ Al phản ứng hết , O2 dư
⇒ Tính toán dựa vào số mol của Al
Số mol của nhôm oxit
nAl2O3 = \(\dfrac{0,2.2}{4}=0,1\left(mol\right)\)
Khối lượng của nhôm oxit
mAl2O3 = nAl2O3 . MAl2O3
= 0,1 . 102
= 10,2 (g)
b) Số mol dư của khí oxi
ndư = nban đầu - nmol
= 0,6 - (\(\dfrac{0,2.3}{4}\))
= 0,45 (mol)
⇒ A = 0,45 . 6 . 10-23 = 2,7 . 10-23 (phân tử)
Chúc bạn học tốt

a)
\(n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\)
Ta thấy :
\(n_{HCl} = 0,2 > 2n_{H_2} = 0,1\) nên HCl dư.
Theo PTHH : \(n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{1}{30}(mol)\\ \Rightarrow m_{Al} = \dfrac{1}{30}.27 = 0,9(gam)\)
Ta có :
\(n_{HCl\ pư} = 2n_{H_2} = 0,1(mol)\\ \Rightarrow n_{HCl\ dư} = 0,2 - 0,1 = 0,1(mol)\\ \Rightarrow m_{HCl\ dư} = 0,1.36,5 = 3,65(gam)\)

1)
a)
PTHH: MgO + 2HCl --> MgCl2 + H2O
=> Số phân tử MgO : số phân tử HCl = 1 : 2
=> Số phân tử HCl = 2.3,6.1023 = 7,2.1023 (phân tử)
b)
Số phân tử MgO : số phân tử MgCl2 = 1 : 1
=> Số phân tử MgCl2 = 3,6.1023 (phân tử)
2)
\(m_{tăng}=m_{KL}-m_{H_2}\)
=> 1,54 = 1,68 - mH2
=> mH2 = 0,14 (g)
=> \(n_{H_2}=\dfrac{0,14}{2}=0,07\left(mol\right)\)
Gọi kim loại cần tìm là R
PTHH: R + 2HCl --> RCl2 + H2
0,07<--------------0,07
=> \(M_R=\dfrac{1,68}{0,07}=24\left(g/mol\right)\)
=> R là Mg

nMg = 6,72 : 22,4 = 0,3 mol
Mg + 2HCl -> MgCl2 + H2
0,3 0,6 0,3
=> mMg = 0,3 . 24 = 7,2 g
CM HCl = 0,6 : 0,5 = 4M

a) nMg = \(\frac{0,3.10^{23}}{6.10^{23}}=0,05\) mol
Pt: Mg + 2HCl --> MgCl2 + H2
0,05 mol------> 0,05 mol-> 0,05 mol
Xét tỉ lệ mol giữa Mg và HCl:
\(\frac{0,05}{1} < \frac{0,3}{2}\)
Vậy HCl dư
Số phân tử H2 sinh ra = 0,05 . 6. 1023 = 0,3 . 1023
b) mMgCl2 = 0,05 . 95 = 4,75 (g)

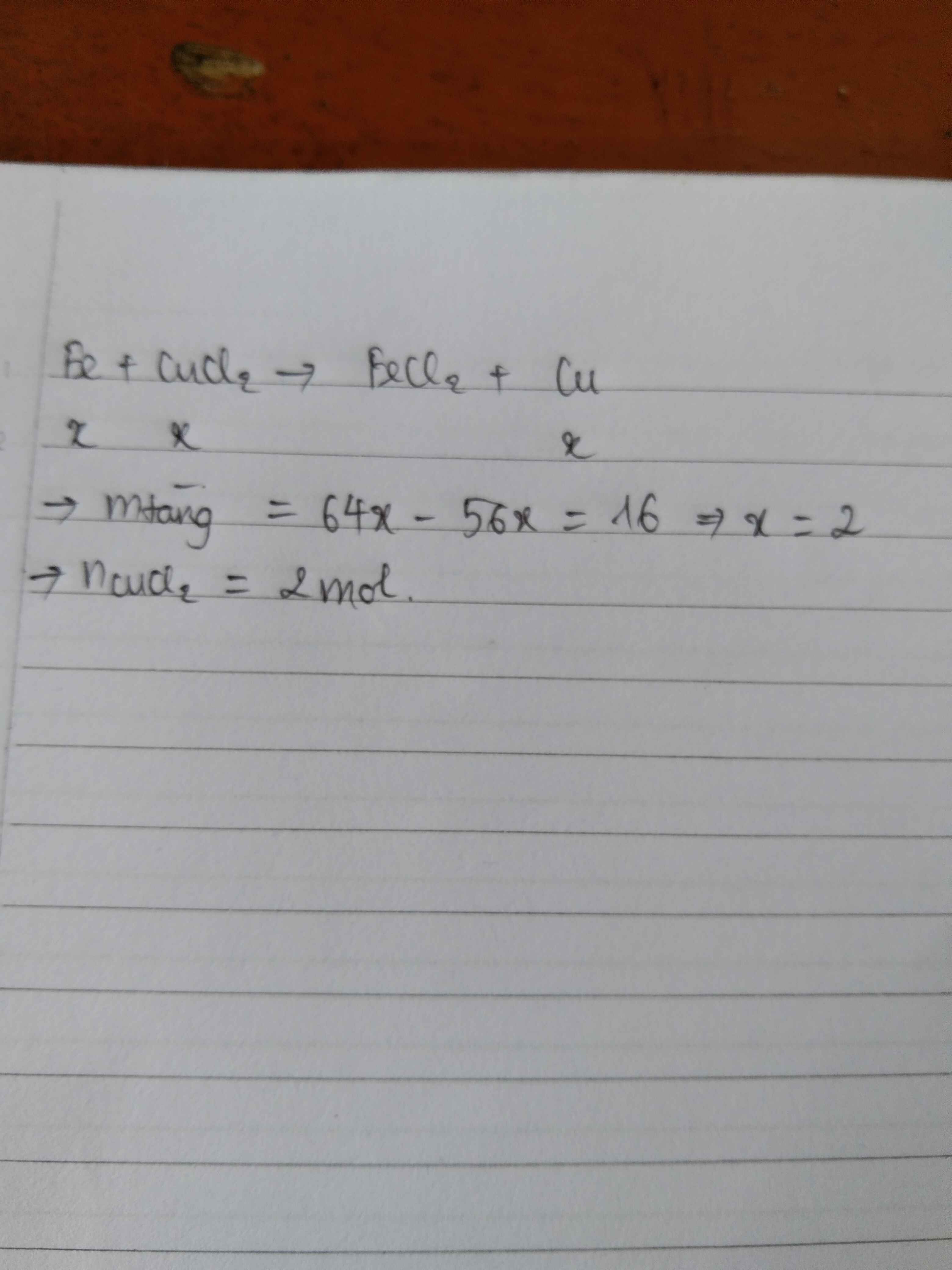
a) Pt: Mg + 2HCl --> MgCl2 + H2
.................0,3 mol->0,15 mol-> 0,15 mol
Số phân tử MgCl2 = 0,15 . 6 . 1023 = 0,9 . 1023
Số phân tử H2 = 0,15 . 6 . 1023 = 0,9 . 1023
b) mMgCl2 = 0,15 . 95 = 14,25 (g)