Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol H2 là 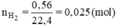
Fe + H2SO4 → FeSO4 + H2
Theo pt nFe = nH2 = 0,025(mol)
→ Khối lượng sắt dùng ở trường hợp 1 là: mFe = 0,025 x 56 = 1,4(g)
TH2: Lượng Fe gấp đôi khi đó số mol Fe là: 0,025. 2 = 0,05 (mol)
Fe + CuSO4 → FeSO4 + Cu
nFe = 0,05 mol.
Khối lượng Fe đã dùng ở trường hợp 2 là: mFe = 0,05 x 56 = 2,8 (g)
Khối lượng chất rắn m = mCu = 0,05 x 64 = 3,2(g)

Gọi a và b lần lượt là số mol của nhôm và của nhôm nitrat.
mX=mnhôm nitrat ⇔ 27a+213b=\(\dfrac{a+b}{2}\).102 ⇔ b=\(\dfrac{4}{27}\)a.
BTe: 3nnhôm=3nNO=3.0,81 ⇒ nnhôm=a=0,81 mol ⇒ b=nnhôm nitrat=0,12 mol.
Rắn khan trong Y chỉ chứa Al(NO3)3 (0,81+0,12=0,93 (mol)) với khối lượng là 0,93.213=198,09 (g).
Chọn B.

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
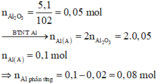
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
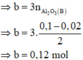
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
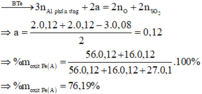

Đáp án A
Ta có sơ đồ phản ứng:
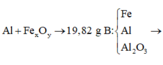
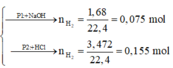
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
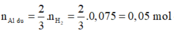
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
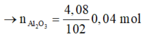
Ta có:
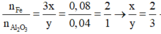
=> Oxit sắt cần tìm là Fe2O3

a) Đặt \(\hept{\begin{cases}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{cases}}\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\) (1)
\(Al+6HNO_3-->Al\left(NO_3\right)_3+3NO_2+3H_2O\) (2)
\(Cu+4HNO_3-->Cu\left(NO_3\right)_2+2NO_2+2H_2O\) (3)
Theo pthh (1) : \(n_{Al}=\frac{2}{3}n_{H_2}=0,2\left(mol\right)\) => \(x=0,2\left(mol\right)\)
Theo ptr (2); (3) : \(n_{NO_2}=3n_{Al}+2n_{Cu}\)
=> \(0,8=0,2\cdot3+2\cdot n_{Cu}\)
=> \(n_{Cu}=0,1\left(mol\right)\)
=> \(a=0,2\cdot27+0,1\cdot64=11,8\left(g\right)\)
b) PTHH : \(NH_3+HNO_3-->NH_4NO_3\) (4)
\(3NH_3+3H_2O+Al\left(NO_3\right)_3-->Al\left(OH\right)_3\downarrow+3NH_4NO_3\) (5)
\(2NH_3+2H_2O+Cu\left(NO_3\right)_2-->Cu\left(OH\right)_2\downarrow+2NH_4NO_3\) (6)
BT Al : \(n_{Al\left(OH\right)_3}=n_{Al}=0,2\left(mol\right)\)
BT Cu : \(n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
=> \(m\downarrow=m_{Al\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=25,4\left(g\right)\)
c) Gọi tên KL là X .
PTHH : \(2Al\left(NO_3\right)_3-t^o->Al_2O_3+6NO_2+\frac{3}{2}O_2\) (7)
\(Cu\left(NO_3\right)_2-t^o->CuO+2NO_2+\frac{1}{2}O_2\) (8)
\(4NO_2+O_2+2H_2O-->4HNO_3\) (9)
\(3X+4nHNO_3-->3X\left(NO_3\right)_n+nNO+2nH_2O\) (10)
viết ptr rồi, nhưng mik có thắc mắc là cho khí B hấp thụ vô nước => tính đc số mol của hno3, rồi áp vô X là ra, nhưng đề lại cho số mol NO =((( hoặc có thể dùng số mol NO để tính nhưng như thế có hơi thừa ko ? tính ra theo 2 cách thì cx ra 2 kq khác nhau ? ai githich giùm mik, hay mik tính sai hoặc phân tích đề sai nhỉ ?? :D

Đặt số mol các chất là
\(\begin{matrix}KClO_3&a&mol\\Ca\left(ClO_3\right)_2&b&mol\\Ca\left(ClO\right)_2&c&mol\\CaCl_2&d&mol\\KCl&e&mol\end{matrix}\)
nO2=\(\dfrac{1}{2}\)nH2SO4=0,78 (mol)
BTKL : mA= mB + mO2 => mB =58,72 (g)
Mà trong B nCaCl2= nK2CO3=0,18 (mol) ( B tác dụng vừa đủ 0,18 mol K2CO3 )
=> B gồm \(\begin{matrix}KCl&0,52&mol\\CaCl_2&0,18&mol\end{matrix}\)
BT K : nKCl (D) = 0,52 + 0,18.2 = 0,88 (mol)
Mà lượng KCl trong D nhiều gấp\(\dfrac{22}{3}\) lần lượng KCl trong A
=> 0,88 = \(\dfrac{22}{3}\)e => e = 0,12 mol
BT K : a + e = 0,52 => a = 0,4
a. Khối lượng kết tủa C : mC=mCaCO3=0,18.100=18 (g)
b. %mKCl=\(\dfrac{0,4.122,5}{83,68}.100\%\approx58,56\%\)
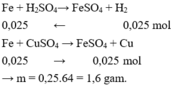
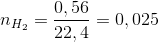 (mol).
(mol).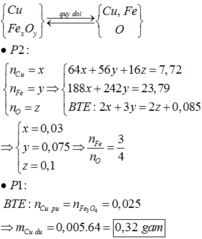
\(TH1.Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ \Rightarrow m_{Fe}=0,025.56=1,4\left(g\right)\\ TH2.Fe+CuSO_4\rightarrow FeSO_4+Cu\\ Lượnggấpđôi:n_{Fe}=0,025.2=0,05\left(mol\right)\\ \Rightarrow m_{Fe}=0,05.56=2,8\left(g\right)\\ n_{Cu}=n_{Fe}=0,05\left(mol\right)\\ \Rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)