Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Coi hỗn hợp X gồm R ( có hoá trị n - a mol) và Fe (b mol)
$\Rightarrow Ra + 56b = 6$
$2R + 2nHCl \to 2RCl_n + nH_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = 0,5an + b = \dfrac{1,85925}{22,4} = 0,083(mol)(1)$
$2R + nCl_2 \xrightarrow{t^o} 2RCl_n$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$m_{Cl_2} = m_{muối} - m_X = 12,39 - 6 = 6,39(gam)$
$n_{Cl_2} = 0,5an + 1,5b = 0,09(2)$
Từ (1)(2) suy ra : an = 0,138 ; b = 0,014
$\%m_{Fe} = a\% = \dfrac{0,014.56}{6}.100\% = 13,07\%$

Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
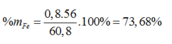

Gọi số mol H2, H2S là a, b (mol)
\(\left\{{}\begin{matrix}a+b=\dfrac{2,24}{22,4}=0,1\\M=\dfrac{2a+34b}{a+b}=9.2=18\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,05 (mol); b = 0,05 (mol)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,05<-------------------0,05
FeS + 2HCl --> FeCl2 + H2S
0,05<---------------------0,05
=> \(\%n_{Fe}=\%n_{FeS}=\dfrac{0,05}{0,05+0,05}.100\%=50\%\)
\(M_{hhkhí}=9.2=18\left(g\text{/}mol\right)\\ n_{hhkhí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Áp dụng sơ đồ đường chéo, ta có:
\(\dfrac{n_{H_2S}}{n_{H_2}}=\dfrac{V_{H_2S}}{V_{H_2}}=\dfrac{34-18}{18-2}=\dfrac{1}{1}\)
\(\rightarrow n_{H_2S}=n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,05<-----------------------0,05
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
0,05<-------------------------0,05
\(\rightarrow\left\{{}\begin{matrix}\%n_{Fe}=\dfrac{0,05}{0,05+0,05}.100\%=50\%\\\%n_{FeS}=100\%-50\%=50\%\end{matrix}\right.\)

Trong Z gồm : \(Mg^{2+}(a\ mol) ; Fe^{2+}(b\ mol) ; Cl^-(2a + 2b\ mol)\)
Ta có : 24a + 56b = 20 - 2(1)
\(Fe^{2+} \to Fe^{3+} + 1e\\ 2Cl^- \to Cl_2 + 2e\\ Mn^{+7} + 5e \to Mn^{+2}\)
Bảo toàn electron :
b + (2a + 2b) = 0,24.5(2)
Từ (1)(2) suy ra a = 0,33 ; b = 0,18
2 gam kim loại còn lại là Fe.
Suy ra:
\(\%m_{Fe} = \dfrac{0,18.56 + 2}{20}.100\% = 60,4\%\)