Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Hấp thụ CO2 vào Ca(OH)2
CO2 + Ca(OH)2 → CaCO3 + H2O
⇒ nCO2 = nCaCO3 = 50 100 = 0,5 mol.
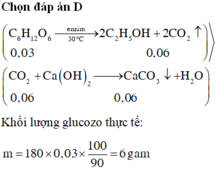
Phản ứng lên men rượu cứ 1C6H12O6 → 2CO2
Theo phương trình
nC6H12O6 lý thuyết = 1 2 × nCO2 = 1 2 × 0,5 = 0,25 mol.
mC6H12O6 lý thuyết = 0,25 × 180 = 45 gam.
Mà H = 87,5% nên mC6H12O6 thực tế = 45 : 0,8 = 56,25

Đáp án D.
n_{Fe_{2}O_{3}}=0,1nFe2O3=0,1 (mol).
Fe2O3 + 3CO -> 2Fe + 3CO2
0,1 0,3
CO2 + Ca(OH)2 -> CaCO3 + H2O
0,3 0,3 (mol)
Vậy m_{CaCO_{3}}mCaCO3 = 100. 0,3 = 30 (gam).
Đáp án D.
(mol).
Fe2O3 + 3CO -> 2Fe + 3CO2
0,1 0,3
CO2 + Ca(OH)2 -> CaCO3 + H2O
0,3 0,3 (mol)
Vậy = 100. 0,3 = 30 (gam).

Tìm ra 2 pt: 84x + 100y + 197z = 20 ; và x + y + z = 0,22.
Thêm vào đó 1 pt là x = a. Ở đây a là 1 số thực và ta chưa biết giá trị của nó (coi như là 1 ẩn số).
==> Ý đồ: tìm a để hệ có nghiệm.
Giải hệ trên: thế x = a vào 2 pt trên ta được:
y + z = 0,22 - a.
100y + 197z = 20 - 84a.
Giải tiếp nữa (dùng pp đại số để giải nha), ta được:
97z = 16a - 2
97y = 23,34 - 113a.
Như vậy để hệ có nghiệm thì y, z >0 ==> 0,125 < a < 23,34/113.
Đó chính là khoảng dao động của x, từ đây thế vào tìm %MgCO3.
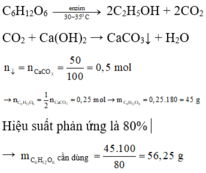
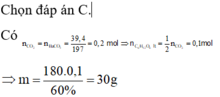
a/
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 0,8 0,8
\(C_6H_{12}O_6\xrightarrow[]{lên.men}2C_2H_5OH+2CO_2\)
0,4 0,8 0,8
\(m_{C_6H_{12}O_6}=0,4.180=72g\)
b/\(V_{CO_2}=0,8.22,4=17,92l\)
c/\(m_{C_2H_5OH}=0,8.46=36,8g\)
nco2 tính sao vậy bạn:(