Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
b, \(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{CuO}=0,8\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,8}{0,1}=8\left(M\right)\)
c, \(n_{H_2}=n_{CuO}=0,4\left(mol\right)\Rightarrow V_{H_2}=0,4.22,4=8,96\left(l\right)\)

Mg+2HCl->MgCl2+H2
0,2----0,4---------------0,2 mol
n Mg=\(\dfrac{4,8}{24}=0,2mol\)ư
=>CmHCl=\(\dfrac{0,4}{0,2}=2M\)
=>VH2=0,2.22,4=4,48l

\(n_{NaOH}=0.2\cdot0.5=0.1\left(mol\right)\)
\(n_{CuSO_4}=0.1\cdot2=0.2\left(mol\right)\)
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
\(0.1.............0.05...............0.05...........0.05\)
\(m_{Cu\left(OH\right)_2}=0.05\cdot98=4.9\left(g\right)\)
\(C_{M_{Na_2SO_4}}=\dfrac{0.05}{0.2+0.1}=0.167\left(M\right)\)
\(C_{M_{CuSO_4\left(dư\right)}}=\dfrac{0.2-0.05}{0.1}=1.5\left(M\right)\)

\(1,n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,3---->0,6------------------>0,3
\(2,C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\\ 3,V_{H_2}=0,3.22,4=6,72\left(l\right)\)

a) Mg + 2HCl ---> H2 + MgCl2
0,25mol 0,25mol 0,25mol 0,25mol
b) + Số mol của HCl:
nHCl = m/M = 18,25/73 = 0,25 (mol)
+ Thể tích của khí H2:
VH2 = n.22,4 = 0,25.22,4 = 5,6 (l)
c) Khối lượng của MgCl2:
mMgCl2 = n.M = 0,25.95 = 23,75 (g)
P/S: 1. Phần in đậm là phần kê mol, sau khi tính mol rồi thì bạn mới kê vào
2. Bài mình giải là mình bỏ chỗ "có lấy dư 20%" đó nha, tại chỗ đó hơi khó hiểu với lại không liên quan đến cách giải thông thường, có gì không rõ nữa thì nhắn hỏi mình ha

\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,05 0,1 0,05
b) \(n_{H2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
100ml = 0,1l
\(C_{M_{HCl}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
Chúc bạn học tốt

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{HCl}=0,15.4=0,6\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Zn}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{ZnCl_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow C_{M_{ZnCl_2}}=\dfrac{0,3}{0,15}=2\left(M\right)\)

\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\\ a,PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ V_{H_2\left(đkc\right)}=0,05.24,79=1,2395\left(l\right)\\ b,n_{HCl}=0,1.3=0,3\left(mol\right)\\ Vì:\dfrac{0,05}{1}< \dfrac{0,3}{2}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,3-0,05.2=0,2\left(mol\right)\\ n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{ddsau}=V_{ddHCl}=0,1\left(l\right)\\ b,C_{MddFeCl_2}=\dfrac{0,05}{0,1}=0,5\left(M\right);C_{MddHCl\left(dư\right)}=\dfrac{0,2}{0,1}=2\left(M\right)\)

\(nFe=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
1 2 1 1 (mol)
0,1 0,2 0,1 0,1 (mol)
m muối là mFeCl2
=> \(mFeCl_2=0,1.127=12,7\left(g\right)\)
\(VH_2=0,1.22,4=2,24\left(l\right)\)
\(VHCl=100ml=0,1\left(l\right)\)
\(CM_{HCl}=\dfrac{nHCl}{VHCl}=\dfrac{0,2}{0,1}=2M\)
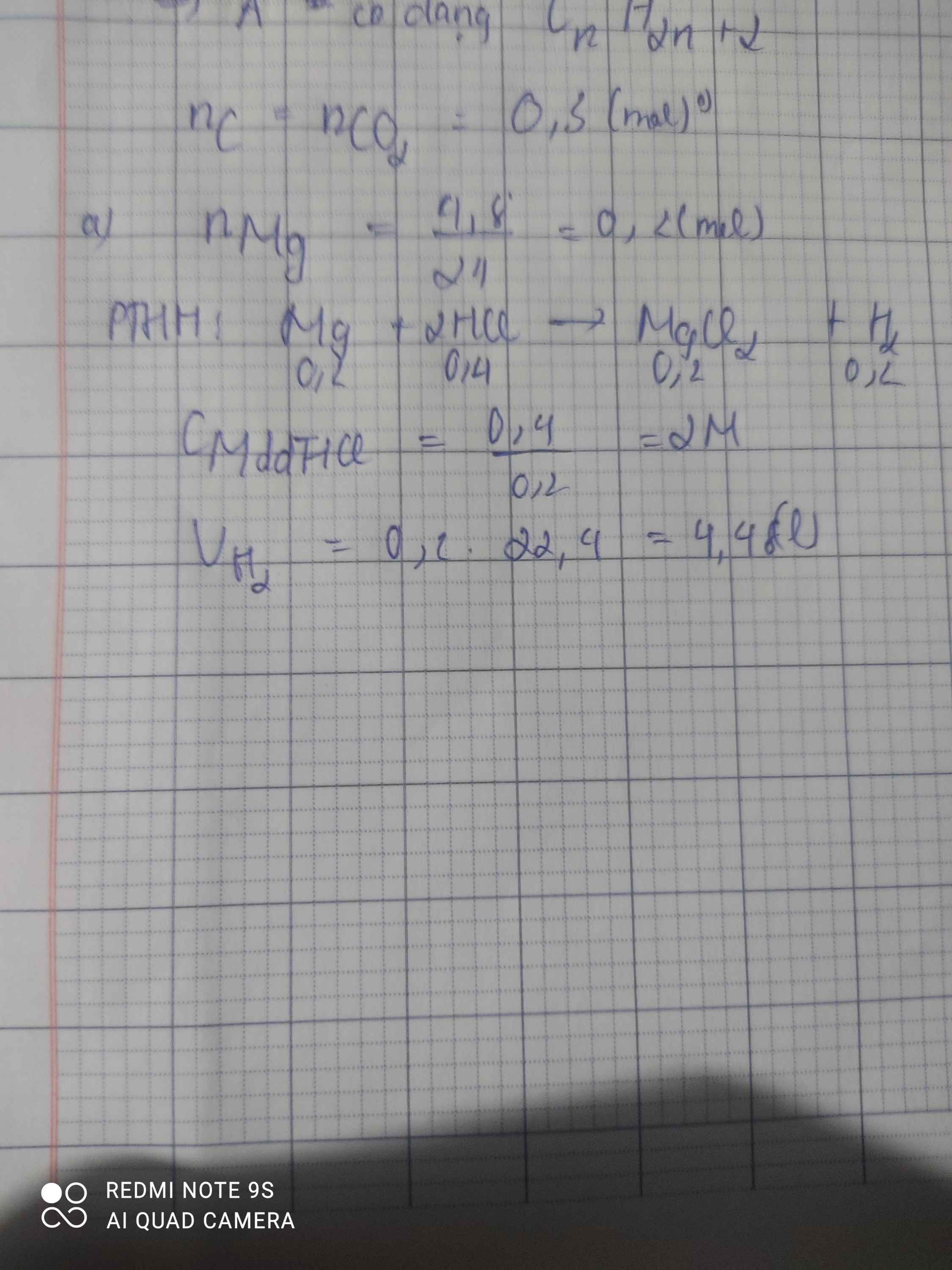
Mg + 2HCl -> MgCl2 + H2
0,1 mol <- 0,2 mol -> 0,1mol
nHCl= 0,1 . 2 = 0,2 mol
Thể tích của Hidro thu được là:
VH2 = 0,1 . 22,4 = 2,24 l
a,Mg + 2HCl → MgCl2 + H2
b, đổi 100ml = 0.1 lít
nHCl= 2 . 0,1 = 0,2 ( mol)
Theo PTHH ta có nH2 = \(\frac{1}{2}\)nHCl = 0,1 (mol)
VH2= 0,1 . 22,4 = 2,24 (l)