Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2xR + yO2 -> 2RxOy
MRxOy=16:40%=40
với y=1 thì x=1 => R là Mg
Với y=2 thì x=ko có giá trị t/m

Phương trình hóa học của phản ứng:
M + n/2HCl → M Cl n
M + mHCl → M Cl m + m/2 H 2
Theo đề bài, ta có:
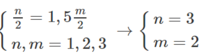
và M + 106,5 = 1,2886 (M+71)
Giải ra, ta có M = 52 (Cr)

a/ A + xAgNO3 \(\rightarrow\) A(NO3)x + xAg
Có : mAg : mA = 12
=> x .108 : MA = 12 => MA = 9x
Biện luận => x= 3 => A là nhôm
b/ Al + FeCl3 -> AlCl3 + Fe
Thấy theo PT : nAl : nFeCl3 = 1: 1
mà cho t/d với tỉ lệ mol 1:2 => FeCl3 dư , Al hết
=> \(\dfrac{m_{Fe}}{m_{Al}}=\dfrac{n.M_{Fe}}{n.M_{Al}}=\dfrac{56}{27}=2,07\)
Vậy khối lượng chất rắn thu được gấp 2,07 lần

Gọi n là hóa trị của A ; \(1\le n\le3\)
Gọi x là số mol của A
\(A+nAgNO_3\rightarrow A\left(NO_3\right)_n+nAg\downarrow\)
x -----------------------------------> xn
theo gt: \(m_{Ag}=12m_A\)
\(\Leftrightarrow108xn=12.xM_A\)
\(\Rightarrow M_A=9n\)
Kẻ bảng.. => n =3 thì MA = 27 ( nhận )
A là Al
\(Al+FeCl_3\rightarrow AlCl_3+Fe\)
x --------------------------> x
\(\dfrac{m_{Fe}}{m_{Al}}=\dfrac{56x}{27x}=2,07\)
=> \(m_{Fe}=2,07m_{Al}\)
\(1\le n\le3\)
| n | 1 | 2 | 3 |
| M | 9 | 18 | 27 |
loại loại nhận
Đối với những ẩn như vậy thì lập bảng ra.

a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3 CO_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$RO + H_2 \xrightarrow{t^o} R + H_2O$
b)
Coi m = 160(gam)$
Suy ra: $n_{Fe_2O_3} = 1(mol)$
Theo PTHH :
$n_{RO} = n_{H_2} = n_{Fe} = 2n_{Fe_2O_3} = 2(mol)$
$M_{RO} = R + 16 = \dfrac{160}{2} = 80 \Rightarrow R = 64(Cu)$
Vậy oxit là CuO

