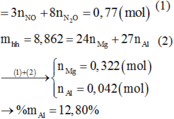Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta đặt nMg= 3x, nAl= 2x mol → mhh= 24.3x+ 27.2x=126x= 5,04 →x=0,04 mol→ nMg= 0,12 mol; nAl= 0,08 mol
Sản phẩm khử gồm 2 khí không màu, không hóa nâu ngoài không khí. Đó là N2 (a mol) và N2O (b mol)
Ta có a+b= 0,896/22,4= 0,04
Và mhh= 28a+ 44b= 18.2.0,04
Giải hệ trên có a= 0,02, b=0,02
QT cho e:
Mg→ Mg2++ 2e
0,12 0,24
Al→ Al3++ 3e
0,08 0,24
Tổng số mol e cho ne cho= 0,24+ 0,24= 0,48 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,2 ← 0,02 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,16 ← 0,02mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,2+ 0,16= 0,36mol <0,48 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,48- 0,36= 0,12 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,12 → 0, 015 mol
Theo các bán phản ứng (2), (3), (4) thì
nNO3-bị khử= 2.nN2+ 2. nN2O+nNH4+= 2.0,02+2.0,02+0,015= 0,095 mol
=nHNO3 bị khử
Đáp án A

nH2=0,1 mol
Fe + 2HCl → FeCl2 + H2
0,1 mol 0,1 mol
mFe=0,1.56=5,6g
%mFe=\(\frac{5,6}{26}\).100=21,5%
m(feo và fe3o4)=26-5,6=20,4g
ta có phương trình cho nhận electron
Fe+2 ---------> Fe+3 + 1e N+5 + 3e-----------> N+2
x mol x mol 0,45 mol 0,15 mol
Fe3+8/3 ------------> 3Fe+3 + 1e
y mol y mol
Fe0 ------------> Fe+3 + 3e
0,1 mol 0,3mol
ta có hệ phương trình
\(\begin{cases}72x+232y+5,6=26\\0,3+x+y=0,45\end{cases}\) =>\(\begin{cases}x=0,09\\y=0,06\end{cases}\)
mFeO=0,09.72=6,48 g %mFeO=\(\frac{6,48}{26}.100=24,9\%\)
mFe3O4=13,92g %mFe3O4= 100%-(21,5%+ 24,9%)=53,6%