Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
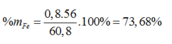

Gọi số mol Mg, Fe, Al là a, b, c
=> 24a + 56b + 27c = 23,8
PTHH: Mg + 2HCl --> MgCl2 + H2
a------------------------->a
Fe + 2HCl --> FeCl2 + H2
b------------------------->b
2Al + 6HCl --> 2AlCl3 + 3H2
c------------------------->1,5c
=> a + b + 1,5c = \(\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
a-->a
2Fe + 3Cl2 --to--> 2FeCl3
b--->1,5b
2Al + 3Cl2 --to--> 2AlCl3
c--->1,5c
=> \(a+1,5b+1,5c=\dfrac{20,16}{22,4}=0,9\left(mol\right)\)
=> a = 0,3; b = 0,2; c = 0,2
=> \(\left\{{}\begin{matrix}m_{Mg}=0,3.24=7,2\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)

Ta có: 53,5nNH4Cl + 132n(NH4)2SO4 = 4,78 (1)
\(n_{NH_3}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
BTNT N, có: nNH4Cl + 2n(NH4)2SO4 = nNH3 = 0,08 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{NH_4}=0,04\left(mol\right)\\n_{\left(NH_4\right)_2SO_4}=0,02\left(mol\right)\end{matrix}\right.\)
⇒ mNH4Cl = 0,04.53,5 = 2,14 (g)
→ Đáp án: C

\(n_{Cl_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(n_{H_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(n_{H_2}=a+1.5b=0.5\left(mol\right)\)
\(n_{Cl_2}=1.5a+1.5b=0.6\left(mol\right)\)
\(\Rightarrow a=b=0.2\)
\(m_X=0.2\cdot\left(56+27\right)=16.6\left(g\right)\)

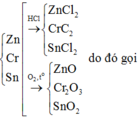
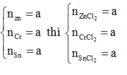

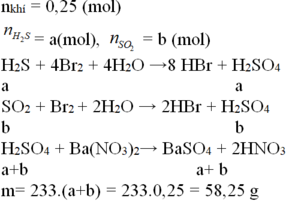


Gọi số mol metan, etilen và axetilen trong X lần lượt là x, y, z.
\(\Rightarrow16x+28y+26z=8,6\)
Cho hỗn hợp X qua dung dịch brom dư
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
\(\Rightarrow n_{Br2}=n_{C2H4}+2n_{C2H2}=y+2z=\frac{48}{80.2}=0,3\left(mol\right)\)
Giả sử lượng 13,44 lít X gấp k lần lượng trên
\(\Rightarrow k.\left(x+y+z\right)=\frac{13,44}{22,4}=0,6\left(mol\right)\)
Cho hỗn hợp tác dụng với AgNO3/NH3
\(C_2H_2+2AgNO_3+2NH_3\rightarrow Ag_2C_2+2NH_4NO_3\)
\(\Rightarrow n_{Ag2C2}=n_{C2H2}=kz=\frac{36}{108.2+12.2}=0,15\left(mol\right)\)
\(\Rightarrow\frac{kz}{k\left(x+y+z\right)}=\frac{0,16}{0,6}\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\\z=0,1\end{matrix}\right.\)
Vì % số mol = % thể tích
\(\Rightarrow\%V_{CH4}=\frac{0,2}{0,2+0,1+0,1}=50\%\)
50%
Trong 8,6g X chứa a mol C2H4; b mol C2H2; c mol CH4
+) mhh X = PT(1)
+) nBr2 phản ứng = nπ trong X = nC2H4 + 2.nC2H2 => PT(2)
+) nC2Ag2 = nC2H2 => %nC2H2 trong X
=> trong 8,6 gam X % số mol C2H2 cũng là 25% => PT(3)
Nếu sai mong bạn bỏ qua .