Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) X + HCl \(\rightarrow\) NO
=> trong X còn muối Fe(NO3)2
\(n_{NO\left(1\right)}=\frac{7,84}{22,4}=0,35mol\); \(n_{NO\left(2\right)}=\frac{1,12}{22,4}=0,05\left(mol\right)\)
Sau khi cho HCl vào X thì thu được dung dịch trong đó chứa: Cu2+ và Fe3+
Gọi x, y lần lượt là số mol của Fe và Cu
Ta có:
\(\begin{cases}56x+64y=26,4\\3x+2y=3\left(0,35+0,05\right)\end{cases}\)\(\Leftrightarrow\begin{cases}x=0,3\\y=0,15\end{cases}\)
=> \(\%Fe=\frac{0,3.56}{26,4}.100\%=63,64\%\); %Cu = 100% - %Fe = 36,36%
2) Số mol HNO3 than gia phản ứng = 4nNO(1) = 0,35.4 = 1,4(mol)
3) Gọi a , b lần lượt là số mol Fe(NO3)2 và Fe(NO3)3 trong X
=> a + b = 0,3
2a + 3b + 2. 0,15 = 3.0,35
=> a = 0,15 (mol); b = 0,15 (mol)
=> trong X có : 0,15 mol Fe(NO3)2; 0,15 (mol) Fe(NO3)3 và 0,15 mol Cu(NO3)2
=> CM các chất đều bằng nhau và bằng: \(\frac{0,15}{0,8}=0,1875M\)

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron

2Cu(NO3)2 → 2CuO + 4NO2↑ + O2↑ (1)
2Mg + O2 → 2MgO (2)
Hỗn hợp rắn X gồm CuO, MgO, Mg dư và Cu(NO3)2
Hỗn hợp X tác dụng với 1,3 mol HCl sinh ra hh Z
Vì sản phẩm khử có H2 nên NO3- pư hết
Áp dụng quy tắc đường chéo ta có:
22,8 20,8 5,2 N2:28 H2:2
\(\frac{nN2}{nH2}=\frac{20,8}{5,2}=\frac{4}{1}=\frac{0,04}{0,01}\)
Bảo toàn nguyên tố O có:
nO(X) = 6nCu(NO3)2 - 2nNO2+O2 = 6.0,25 - 2.0,45 = 0,6 (mol)
Xét phản ứng trao đổi giữa H+ và O(trong X)
2H+ + O-2 → H2O
0,6 → 0,6 (mol)
=> nH2O = nO(X) = 0,6 (mol)
BTNT "H": nHCl = 4nNH4+ + 2nH2 + 2nH2O
=> 1,3 = 4nNH4+ + 2.0,01 + 2.0,6
=> nNH4+ = 0,02 (mol)
Dung dịch muối thu được gồm: NH4+: 0,02 (mol); Cu+2: 0,25 (mol); Cl-: 1,3 (mol): Mg2+: a (mol)
Bảo toàn điện tích ta có: nNH4+ + 2nCu2+ + 2nMg+2 = nCl-
=> 0,02 + 2.0,25 + 2a = 1,3
=> a = 0,39 (mol)
=> m muối = 0,02.18 + 0,25.64 + 1,3.35,5 + 0,39.24 = 71,87 (g)
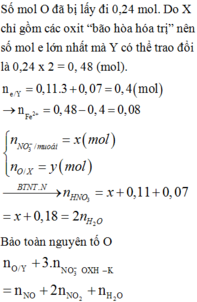
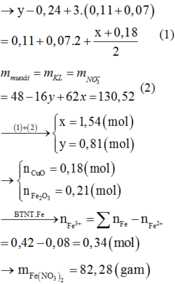
Chọn đáp án C