Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
Zn + 2HCl \(\rightarrow\)ZnCl2 + H2 (1)
Fe + 2HCl \(\rightarrow\)FeCl2 + H2 (2)
nH2=\(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Vì Cu không tan trong axit bình thường nên chất rắn là Cu
mCu=3(g)
Đặt nZn=a
nFe=b
Ta có:
\(\left\{{}\begin{matrix}65a+56b=18,6\\a+b=0,3\end{matrix}\right.\)
=>a=0,2;b=0,1
mZn=65.0,2=13(g)
mFe=56.0,1=5,6(g)
2.
Gọi CTHH của oxit là MO
MO + 2HCl \(\rightarrow\)MCl2 + H2
mHCl=30.\(\dfrac{14,6}{100}=4,38\left(g\right)\)
nHCl=\(\dfrac{4,38}{36,5}=0,12\left(mol\right)\)
Theo PTHH ta có:
\(\dfrac{1}{2}\)nHCl=nMO=0,06(mol)
MMO=\(\dfrac{4,8}{0,06}=80\)
MM=80-16=64
Vậy M là Cu,CTHH của oxit là CuO

B3: Gọi M là tên kim loại hóa trị III=>oxit của nó là M2O3
mct(H2SO4)=294*20/100=58.8(g)
=>nH2SO4=58.8/98=0.6(mol)
M2O3+3H2SO4=>M2(SO4)3+3H2O
0.2----->0.6(mol)
=>nM2O3=0.6/3=0.2(mol)
=>M2O3=32/0.2=160(g)
=>M=160-48/2=56(g)=>Fe
Vậy công thức của oxit kim loại là Fe2O3.

PTHH: R + 2HCl --> RCl2 + H2
R + 2HCl --> RCl2 + H2O
Đổi : 200 ml = 0,2 l
Nồng độ mol HCl là: CM = n : V = nhcl : 0,2 = 2
=> Số mol HCl là : 0,2 . 2 = 0,4 ( mol )
Tổng khối lượng HCl là : 0,4 . 36,5 = 14,6 ( gam )
a) Số mol của Hiđro là : 2,24 : 22,4 = 0,1 ( mol )
=> Số mol HCl ở pt (1) là: 0,1 . 2 = 0,2 ( mol )
=> Số mol HCl ở pt (2) là : 0,4 - 0,2 = 0,2 ( mol )
( Vì tổng số mol HCl ở cả 2 pt là 0,4 mol )
- Theo đề bài ra ta có: Tổng khối lượng RCl2 Cả 2 PT Là 27,2 gam .... ( PTK của Cl2 : 71 )
<=> 0,1 . ( MR + 71 ) + 0,1 . ( MR + 71 ) = 27,2
<=> 0,2 MR + 7,1 + 7,1 = 27,2
<=> MR = 65
=> R là Zn ( Kẽm )
b) Số mol H2O là : 0,2 : 2 = 0,1 ( mol )
Khối lượng của H2O là : 0,1 . 18 = 1,8 ( gam )
- áp dụng định luật bảo toàn khối lượng ta có:
m + 14,6 = 27,2 + 1,8 + 0,2
<=> m = 14,6 ( gam )

\(n_{Fe_2O_3}=n_{FeO}=n_{Fe_3O_4}=a\\ n_{NO_2}:n_{NO}=\dfrac{46-34}{34-30}=3\\ n_{NO_2}+n_{NO}=\dfrac{4,48}{22,4}=0,2\\ n_{NO_2}=0,15;n_{NO}=0,05\\ BTe:a+a=0,15+0,15\\ a=0,15\\ m_A=a\left(160+232+72\right)=69,6g\\ BT\left[N\right]:V_{HNO_3}=\dfrac{6a\cdot3-0,2}{2}=1,25L\)

_Quy đổi hh chỉ gồm FeO và Fe2O3
_Cho hh td vs dd H2SO4 dư:
FeO + H2SO4 ->FeSO4 + H2O (1)
Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O (2)
_dd X gồm H2SO4 dư, FeSO4 và Fe2(SO4)3
_Gọi số mol của FeSO4 và Fe2(SO4)3 lần lượt là 2x và 2y (x,y > 0)
_Theo bài:
m1/2 X = mFeSO4 + mFe2(SO4)3
=> 67,48 = 152x + 400y (*)
_Phần 2 : Cho td vs dd KMnO4
10FeSO4 + 8H2SO4 + 2KMnO4 ->2MnSO4 + K2SO4 + 5Fe2(SO4)3 + 8H2O
_Theo bài:
nKMnO4 = 0,5 . 0,046 = 0,023 mol
=> x = nFeSO4 = 5.nKMnO4 = 5 . 0,023 = 0,115 mol
=> nFeSO4 bđ = 2 . 0,015 = 0,23 mol
=>nFeO = nFeSO4 bđ = 0,23 mol
=>mFeO = 0,23 . 72 = 16,56 g
Thay x = 0,115 vào (*) ta đc:
152 . 0,015 + 400y = 67,48
=> 400y = 50 (chỗ này hơi tắt nhưng bn tự diễn giải ra nha)
=>y = 0,125
=>nFe2(SO4)3 bđ = 2.0,125 = 0,25 mol
=>nFe2O3 = nFe2(SO4)3 = 0,25 mol
=>mFe2O3 = 0,25 . 160 = 40g
=>m hh bđ = 16,56 + 40 = 56,56 g
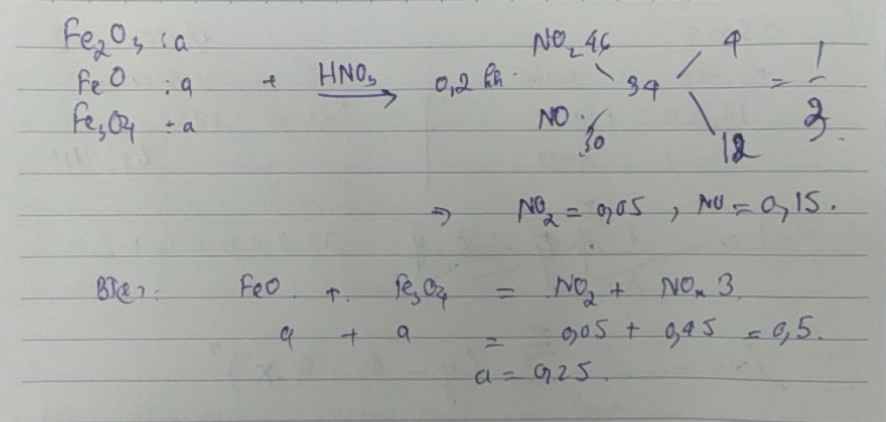
Ta có: \(n_{HCl}=2.\dfrac{200}{1000}=0,4\left(mol\right)\)
PTHH:
\(Fe+2HCl--->FeCl_2+H_2\uparrow\left(1\right)\)
\(MO+2HCl--->MCl_2+H_2O\left(2\right)\)
Gọi x, y lần lượt là số mol của Fe và MO
Theo PT(1): \(n_{HCl}=2.n_{Fe}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{MO}=2y\left(mol\right)\)
\(\Rightarrow2x+2y=0,4\) (*)
Theo đề, ta có: \(56x+My+16y=11,2\) (**)
Từ (*) và (**), ta có:
\(\left\{{}\begin{matrix}2x+2y=0,4\\56x+16y+My=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}16x+16y=3,2\\56x+16y+My=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}40x+My=8\\2x+2y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}40x+My=8\\40x+40y=8\end{matrix}\right.\Leftrightarrow M=40\)
Vậy M là nguyên tử canxi (Ca)