Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

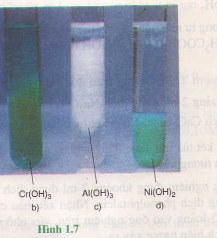
CrCl3 + 3NaOH (đủ) → Cr(OH)3 ↓ + 3 NaCl
Cr3+ + 3OH- → Cr(OH)3 ↓
AlCl3 + 3NaOH (đủ) Al(OH)3 ↓ + 3 NaCl
Al3+ + 3OH- → Al(OH)3 ↓
Hoặc AlCl3 + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4Cl
Al3+ + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4+
Ni(NO3)2 + 2NaOH → Ni(OH)2 ↓ + 2NaNO3
Ni2+ + 2OH- → Ni(OH)2 ↓

Cr(NO3)3 + 3NaOH(vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KC1 ;
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3.

Cr(NO3)3 + 3NaOH(vừa đủ) → Cr(OH)3↓ + 3NaNO3 ;
AlCl3 + 3KOH (vừa đủ) → Al(OH)3↓ + 3KC1 ;
Ni(NO3)2 + 2NaOH → Ni(OH)2↓+ 2NaNO3.
nhìn cái ảnh này là thể hiện tự đăng rồi. Bữa trước môn sinh cũng thế chứ đâu

a)
$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
$n_{BaCl_2} = 0,01 = n_{Na_2SO_4} = 0,01 \Rightarrow $ Vừa đủ
$n_{BaSO_4} = n_{Na_2SO_4} = 0,01(mol)$
$m_{BaSO_4} = 0,01.233 = 0,233(gam)$
b)
$n_{NaCl} = 2n_{Na_2SO_4} = 0,02(mol)$
$V_{dd} = 0,1 + 0,2 = 0,3(lít)$
$C_{M_{NaCl}} = \dfrac{0,02}{0,3} = 0,067M$
c)
$[Na^+] = [Cl^-] = C_{M_{NaCl}} = 0,067M$
\(n_{BaCl_2}=0.1\cdot0.1=0.01\left(mol\right)\)
\(n_{Na_2SO_4}=0.2\cdot0.05=0.01\left(mol\right)\)
\(BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\)
\(0.01..........0.01............0.01..............0.02\)
\(m_{BaSO_4}=0.01\cdot233=2.33\left(g\right)\)
\(C_{M_{NaCl}}=\dfrac{0.01}{0.1+0.2}=0.03\left(M\right)\)
\(\left[Na^+\right]=\left[Cl^-\right]=0.03\left(M\right)\)

Đáp án C. Vì chỉ rõ các ion nào đã tác dụng với nhau làm cho phản ứng xảy ra.

1. 2 N H 4 + + S O 4 2 - + B a 2 + + 2 O H - → B a S O 4 ↓ + 2 N H 3 ↑ + 2 H 2 O
2. Số mol B a S O 4 : 17,475/233 = 0,075(mol)
Theo phản ứng, vì lấy dư dung dịch B a ( O H ) 2 nên S O 4 2 - chuyển hết vào kết tủa B a S O 4 và N H 4 + chuyển thành N H 3 . Do đó :
n S O 4 2 - = n B a S O 4 = 0,075 mol ;
n N H 4 + = 2. n S O 4 2 - = 2. 0,075 = 0,15 (mol).
Nồng độ mol của các ion N H 4 + và S O 4 2 - trong 75 ml dung dịch muối amoni sunfat :
[ N H 4 + ] = 2 (mol/l)
[ S O 4 2 - ] = 1 (mol/l)