Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D
nSO42- = nBaSO4 = 0,1 ⇒ [(NH4)2SO4] = 0,1/0,1 = 1M
nNH3 = 0,3 = nNH4+
Bảo toàn điện tích ⇒ nNH4+ = 2nSO42- + nNO3- ⇒ nNO3- = 0,3 – 2.0,1 = 0,1
⇒ [NH4NO3] = 0,1/0,1 = 1M

Chọn A
nOH- = 0,06x2 = 0,12 > nNH3 = 0,08 Þ OH- dư Þ Trong X có chứa nNH4+ = 0,08
BTĐT => n S O 4 2 - = (0,12 + 0,08 - 0,l)/2 = 0,05 < nBa2+ = 0,06 Þ Có 0,05 mol BaSO4 kết tủa
Þ Trong Z có nBa2+ = 0,06 - 0,05 = 0,01; nK+ = 0,12; nCl- = 0,1; nOH- = 0,12 - 0,08 = 0,04
Vậy m = 0,01x137 + 0,12x39 + 0,1x35,5 + 0,04x17 = 10,28.

Chọn A.
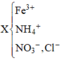

![]()
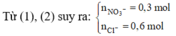
Khi cho X tác dụng với H2SO4 thì dung dịch thu được có chứa Fe3+ (0,2); NO3– (0,3); H+ dư.
Khi cho Cu tác dụng với dung dịch trên thì:
![]()
![]()
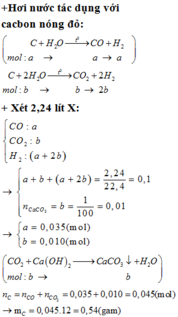

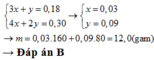


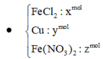
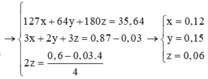
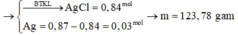
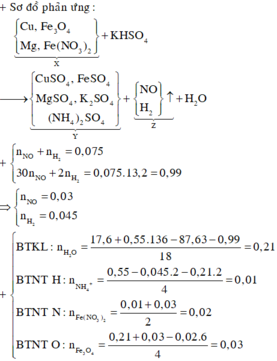

Đáp án A