Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

TL:
Glyxin: H2N-CH2-COOH (75 g/mol), axit cacboxylic: R(COOH)n.
Phần 1: Khi cho hh X phản ứng với NaOH thì muối thu được gồm: H2N-CH2-COONa và R(COONa)n.
Khí Y khi cho đi qua Ca(OH)2 dư thì CO2 và H2O bị hấp thụ còn N2 thoát ra ngoài. Do đó khối lượng tăng lên 20,54 g chính là khối lượng của hh CO2 và H2O.
Mặt khác: CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O, số mol của CaCO3 là 0,34 mol = số mol của CO2.
Suy ra, khối lượng của H2O = 20,54 - 44.0,34 = 5,88 g.
Như vậy, có thể thấy trong 1/2 hh X gồm có các nguyên tố (C, H, O, và N). Theo định luật bảo toàn nguyên tố ta có:
số mol của C = n(CO2) + n(Na2CO3) = 0,34 + 0,1 = 0,44 mol.
số mol của H = 2n(H2O) + nNa = 2.5,58/18 + 2.0,1 = 0,82 mol.
số mol của O = 2nNa = 0,4 mol.
Phần 2: Khi cho phản ứng với HCl chỉ có glyxin tham gia phản ứng: H2N-CH2-COOH + HCl \(\rightarrow\) ClH3N-CH2-COOH. Số mol của glyxin = số mol của HCl = 0,04 mol.
Do đó, trong 1/2 hh X thì số mol của N = 0,04 mol.
Như vậy, khối lượng của 1/2 hh X = mC + mH + mO + mN = 12.0,44 + 0,82.1 + 16.0,4 + 0,04.14 = 13,06 gam.
Khối lượng của glyxin trong 1/2 hh X = 75.0,04 = 3 gam.
Phần trăm khối lượng của glyxin trong hh X = 3/13,06 x 100% = 22,97%. (đáp án D).

BL
CO2+Ca(OH)2==>CaCO3+H20
0.07<= 0.07
đây là bài toán lừa đó bạn ạ . hóa trị của KL thay đổi nên gọi n m lan luot la hoa trị trong oxit và trong KL
ta gọi KL la M
M+ nHCL= MCLm+ (n/2) H2
1.76/22.4
từ PT khử thành KL áp dụng định luật BTKL ta có
mM=4.06+0.07*28-0.07*44=2.94 g
==> M=18.7n
xét từng trường hợp => M=56==> Fe . CT oxit Fe3O4
Chúc bn học tốt![]()

1)2 Al +6HCl--->2AlCl3 +3H2
Fe +2 HCl --->FeCl2 +H2
2) đặt nAl=x,nFe=y =>từ phương trình ở ý 1) và theo bài ra ta có;3/2.x+y=4.48/22.4 và 27x+56y=5.5.giải hệ hai phương trình=>x=0.1 và y=0.05=>mAl=27.0.1=2.7(gam)=>% về khối lượng của Al trong hỗn hợp=(2.7/5.5).100%=49.1%=>%về khối lượng của Fe trong hỗn hợp=100%-49.1%=50.9%.
3) pt : CuO + H2----> Cu +H2O.ta có nH2=0.2(mol),nCuO=0.1(mol)=>CuO pư hết và H2 dư=> nCu=nCuO=>mCuO=0.1 nhân 64=6.4 (gam).


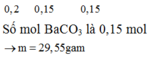





Chọn D.
Ta có: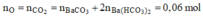
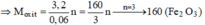
Khi cho Fe tác dụng với HCl thì: