Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình ion rút gọn :
a) Ca2+ + CO32- → CaCO3 ↓
b) Fe2+ + 2OH- → Fe(OH)2↓
c) HCO3- + H+ → CO2 ↑ + H2O
d) HCO3- + OH- → H2O + CO32-
e) Không có phương trình ion rút gọn.
g) Pb(OH)2(r) + 2H+ → Pb2+ + 2H2O
h) H2PbO2(r) + 2OH- → PbO22- + 2H2O
i) Cu2+ + S2- → CuS↓.

Phương trình phân tứ và ion xảy ra trong dung dịch :
a) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3\(\downarrow\) + 3Na2SO4
2Fe3+ + 3SO42- + 6Na+ + 6OH- → 2Fe(OH)3\(\downarrow\)+ 6Na+ + 3SO42-
Fe3+ + 3OH- → Fe(OH)3\(\downarrow\)
b) NH4Cl + AgNO3 → NH4NO3 + AgCl↓
NH4 + Cl- + Ag+ + NO3- → NH4+ + NO3- + AgCl↓
Cl- + Ag+ → AgCl↓
c) NaF + HCl → NaCl + HF↑
Na+ + F- + H+ + Cl- → Na+ + Cl- + HF↑
F- + H+ → HF\(\uparrow\)
d) Không có phản ứng xảy ra
e) FeS(r) + 2HCl → FeCl2 + H2S ↑
FeS(r) + 2H+ + 2Cl- → Fe2+ + 2Cl- + H2S↑
FeS(r) + 2H+ \(\rightarrow\) Fe2+ + H2S↑
g) HClO + KOH \(\rightarrow\) KClO + H2O
HClO + K+ + OH- \(\rightarrow\) K+ + CIO- + H2O
HClO + OH- \(\rightarrow\) CIO- + H2O.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 \(\rightarrow\) Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 \(\rightarrow\) H+ + NO-3
0,020M 0,020M 0,020M
KOH \(\rightarrow\) K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

Khối lượng bình (1) tăng 0,63g chính là khối lượng H2O.
\(\Rightarrow m_H=\frac{0,63}{18}.2=0,07g\)
Ở bình (2) : \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(0,05\leftarrow\frac{5}{100}=0,05\)
\(\Rightarrow m_C=0,05.12=0,6g\)
\(\Rightarrow m_O=0,67-\left(m_C+m_H\right)=0\)
\(\Rightarrow\%m_C=\frac{0,6}{0,67}.100=89,55\%\)
\(\%m_H=100\%-89,55\%=10,45\%\)
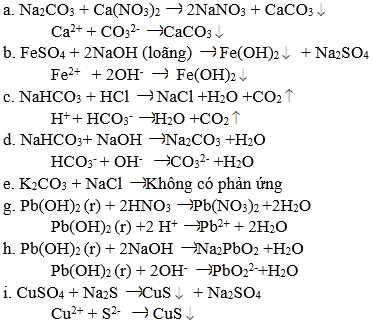
Đáp án D
Tỉ khối hỗn hợp khí với H2 tăng => chứng tỏ số mol khí giảm ( vì khối lượng trước phản ứng và sau phản ứng không đổi) => phản ứng dịch chuyển theo chiều thuận
Các yếu tố thỏa mãn là (1) và (4)