Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Các nhóm đẩy electron ( ankyl) làm tăng mật độ electron trên nguyên tử N → làm tăng tính bazo so với NH3 → Tính bazo (CH3)2NH > CH3NH2 > NH3
Các nhóm hút electron (C6H5) làm giảm mật độ electron làm giảm tính bazo so với NH3 → C6H5NH2 < NH3
Vậy tính bazo C6H5NH2 < NH3 < CH3NH2 < (CH3)2NH
Axit liên hợp tương ứng có tính axit đảo lại : C6H5NH2 > NH3 > CH3NH2 > (CH3)2NH
Axit càng mạnh thì pH càng nhỏ → giá trị của pH (2)< (1) < (4) < (3).

Đáp án C
Các nhóm đẩy electron ( ankyl) làm tăng mật độ electron trên nguyên tử N → làm tăng tính bazo so với NH3 → Tính bazo (CH3)2NH > CH3NH2 > NH3
Các nhóm hút electron (C6H5) làm giảm mật độ electron làm giảm tính bazo so với NH3 → C6H5NH2 < NH3
Vậy tính bazo C6H5NH2 < NH3 < CH3NH2 < (CH3)2NH
Axit liên hợp tương ứng có tính axit đảo lại : C6H5NH2 > NH3 > CH3NH2 > (CH3)2NH
Axit càng mạnh thì pH càng nhỏ → giá trị của pH (2)< (1) < (4) < (3). Đáp án C.

Đáp án : B
Cùng pH nghĩa là cùng số mol H+ phân li ra. Nồng độ mol càng cao, H+ phân li ra càng nhiều và axit càng mạnh, H+ cũng càng phân li ra nhiều.
Do đó HCl là axit mạnh nhất nên cũng phân li ra nhiều H+ nhất, do đó HCl có nồng độ thấp nhất => Loại C và D
C6H5NH3Cl có tính axit mạnh hơn NH4Cl do có nhóm C6H5-
=> thứ tự đúng là
HCl < C6H5NH3Cl < NH4Cl
=> Đáp án B

Đáp án C
Các cặp chất xảy ra phản ứng ở nhiệt độ thường là:
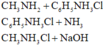
Tính bazo càng yếu thì
Tính bazo càng yếu thì tính axit càng mạnh

Chọn A
Nhận thấy lực bazơ tăng dần theo thứ tự (4) < (1) <(2) <(3) → pH cũng tăng dần theo chiều (4) < (1) <(2) <(3).

Đáp án D
4 chất thỏa mãn điều kiện là H2NCH(CH3)COOH; C6H5OH (phenol); CH3COOC2H5; CH3NH3Cl
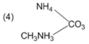
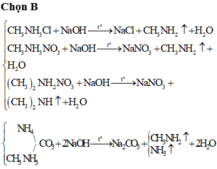
Chọn C
Cả 4 đáp án được tạo bởi gốc cation bazơ yếu và anion axit -Cl mạnh nên đều có pH < 7.
Xét về lực bazơ (CH3)2NH > CH3NH2 > NH3 > C6H5NH2
⇒ (CH3)2NH2Cl có tính bazơ mạnh nhất ⇒ pH lớn nhất.