Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi % đồng vị 21H là a: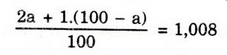
⇒ a = 0,8;
Khối lượng riêng của nước 1 g/ml, vậy 1ml nước có khối lượng 1g. Khối lượng mol phân tử của nước là 18g.


\(Q_{5,03\left(g\right)}=mc\Delta t=100cm^3\cdot0,9969g\cdot cm^{-3}\cdot4,2J\cdot g^{-1}\cdot K^{-1}\cdot\left(34,7-23\right)K\\ Q\approx4900J=4,9kJ\\ Q_{kJ\cdot mol^{-1}}=\dfrac{4,9kJ}{\dfrac{5,03g}{39g\cdot mol^{-1}}}=38kJ\cdot mol^{-1}\)

Đặt công thức của tinh thể ngậm nước tách ra là MgSO4.nH2O
Trong 120 + 18n gam MgSO4.nH2O có 120 gam MgSO4 và 18n gam H2O
1,58 gam 0,237n gam
Khối lượng các chất trong 100 gam dung dịch bão hoà:
\(m_{H_2}=\frac{100.100}{35,1+100}=74,02g\)
\(m_{MgSO_4}=\frac{100.35,1}{35,1+100}\) = 25,98 gam
Khối lượng các chất trong dung dịch sau khi kết tinh:
\(m_{H_2O}\) = 74,02 – 0,237n gam
\(m_{MgSO_4}\)= 25,98 + 1 – 1,58 = 25,4 gam
Độ tan: s = \(\frac{25,4}{74,02-0,237n}.100=35,1\) . Suy ra n = 7.
Vậy công thức tinh thể ngậm nước kết tinh là MgSO4.7H2O

Đáp án D
(1) Phản ứng tỏa nhiệt, tăng nhiệt độ -> Chuyển dịch chiều nghịch
(2) Tăng áp suất -> Chuyển dịch k chuyển dịch
(3) Thêm hơi nước -> Chuyển dịch chiều thuận
(4) Lấy bớt H2 -> Chuyển dịch chiều thuận
(5) Xúc tác k làm chuyển dịch cân bằng
-> D

