Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Coi như hỗn hợp X chỉ gồm Na, K, Ba, O
Cho X vào nước thì 3 kim loại phản ứng sinh ra khí H2, còn O tác dụng với H2 để tạo ra nước theo tỷ lệ 1Oxi+1H2
\(\Rightarrow\) \(n_{H_2}=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_O=0,14\left(mol\right)\)
Có \(n_{Na}=n_{NaOH}=0,18\left(mol\right)\)
\(n_K=n_{KOH}=\frac{0,044m}{56};n_{Ba}=n_{Ba\left(OH\right)_2}=\frac{0,93m}{171}\left(mol\right)\)
\(\Rightarrow n_O=\frac{1}{2}n_{Na}+\frac{1}{2}n_K+n_{Ba}-n_{H_2}=0,09+\frac{0,022m}{56}+\frac{0,465m}{171}\)
Lại có phương trình tổng khối lượng hỗn hợp X:
\(m_X=m=m_{Na}+m_K+m_{Ba}+m_O\\ =0,18.23+\frac{0,044m}{56}.39+\frac{0,93m}{171}.137+m_O\)
Thay số mol Oxi tính được (theo m) ở trên vào ta được phương trình 1 ẩn m
giải ra được \(m\approx25,5\)

Đáp án A
%mO/X = 86,3×0,1947 = 16,8 gam.
⇒ nO = 1,05 ⇒ nAl2O3 = 0,35 mol.
Ta có ∑nOH– = 2nH2 = 1,2 mol.
⇒ Dung dịch Y chứa nAlO2– = nAl/Al2O3 = 0,7 mol || nOH dư = 0,5 mol.
+ Sau phản ứng trung hòa nH+ = 3,2×0,75 – 0,5 = 1,9 mol
⇒ nAl(OH)3 = 0,7 – 1 , 9 - 0 , 7 3 = 0,3 mol.
+ Cho 0,3 mol Al(OH)3 phản ứng với KOH ta có phản ứng:
Al(OH)3 + KOH → KAlO2 + 2H2O ||⇒ nKOHcần dùng = 0,3.
⇒ VKOH = 0 , 3 1 , 25 = 0,24 lít = 240 ml

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Đáp án B
mO = 84 × 0,2 = 16,8 gam ||⇒ nO = 1,05 mol
⇒ nAl2O3 = 0,35 mol.
nOH = 2nH2 = 1,2 mol || Al2O3 + 2OH–
→ 2AlO2– + H2O ||⇒ OH– dư.
nAlO2– = 0,35 × 2 = 0,7 mol; nOH– dư = 1,2 – 0,35 × 2 = 0,5 mol.
nH+ = 3,2 × 0,75 = 2,4 mol || H+ + OH– → H2O ||
⇒ nH+ dư = 2,4 – 0,5 = 1,9 mol.
H+ + AlO2– + H2O → Al(OH)3↓; Al(OH)3 + 3H+ → Al3+ + 3H2O.
⇒ nAl(OH)3 = (4 × 0,7 – 1,9) ÷ 3 = 0,3 mol
⇒ m = 0,3 × 78 = 23,4 gam

Đáp án A
mO = 84 × 0,2 = 16,8 gam ||⇒ nO = 1,05 mol ⇒ nAl2O3 = 0,35 mol.
nOH = 2nH2 = 1,2 mol || Al2O3 + 2OH– → 2AlO2– + H2O ||⇒ OH– dư.
nAlO2– = 0,35 × 2 = 0,7 mol; nOH– dư = 1,2 – 0,35 × 2 = 0,5 mol.
nH+ = 3,2 × 0,75 = 2,4 mol || H+ + OH– → H2O ||⇒ nH+ dư = 2,4 – 0,5 = 1,9 mol.
H+ + AlO2– + H2O → Al(OH)3↓; Al(OH)3 + 3H+ → Al3+ + 3H2O.
⇒ nAl(OH)3 = (4 × 0,7 – 1,9) ÷ 3 = 0,3 mol ⇒ m = 0,3 × 78 = 23,4 gam.

Đáp án A
![]()
Từ số mol H2 ta tính được số mol O H - (giải thích:
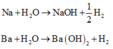
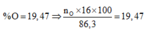
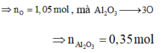
![]()
Ta có phương trình:
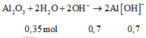
=> dung dịch Y gồm
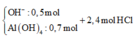
![]()
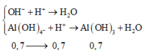
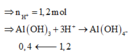
=> Số mol kết tủa còn lại là:
![]()

 với các chất sau:
với các chất sau: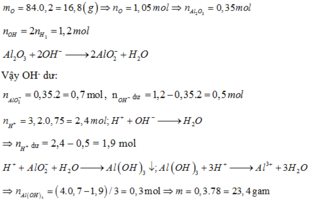
Giải thích:
mO=8,63.19,47/100=1,68 gam=>nO=0,105 mol=>nAl2O3=0,035 mol
nOH-=2nH2=0,12 mol
Al2O3+2OH- → AlO2-+H2O
0,035 0,07(dư 0,05) 0,035
H+ + OH- → H2O
0,05←0,05
H+ + AlO2- + H2O → Al(OH)3
0,07← 0,07 0,07
Al(OH)3+3H+ → Al3+ + H2O
0,04 ←0,12
nAl(OH)3=0,07-0,04=0,03 mol=>m↓=0,03.78=2,34 gam.
Đáp án A