Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
n M n O 2 = 69 , 6 87 =0,8 (mol); n N a O H = 0,5.4 = 2 (mol)
M n O 2 + 4HCl → M n C l 2 + C l 2 + 2 H 2 O
0,8 0,8 (mol)
C l 2 + 2NaOH → NaCl + NaClO + H 2 O
0,8 1,6 0,8 (mol)
C M N a C l = 0 , 8 0 , 5 = 1,6(M); C M ( N a O H d ư ) = 2 - 1 ; 6 0 ; 5 = 0,8(M)

Đáp án C
![]() = 0,8 mol
= 0,8 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 → ![]() = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M

MnO2 + 4HCl\(\rightarrow\) MnCl2 + Cl2 + 2H2O
Ta có : nMnO2=\(\frac{69,6}{\text{55+16.2}}\)=0,8 mol
Theo ptpu: nCl2=nMnO2=0,8 mol
nNaOH=0,5.4=2 mol
Cho Cl2 vào dung dịch NaOH
2NaOH + Cl2\(\rightarrow\) NaCl + NaClO + H2O
Vì nNaOH > 2nCl2 nên NaOH dư
\(\rightarrow\) nNaOH phản ứng=2nCl2=0,8.2=1,6 mol
\(\rightarrow\) nNaOH dư=2-1,6=0,4 mol
nNaCl=nNaClO=nCl2=0,8 mol
\(\rightarrow\)CM NaOH dư=\(\frac{0,4}{0,5}\)=0,8M
CM NaCl= CM NaClO=\(\frac{0,8}{0,5}\)=1,6M

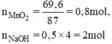
a) Phương trình hóa học của phản ứng:
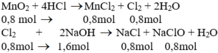
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 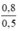 = 1,6 mol/ lit
= 1,6 mol/ lit
CM (NaOH)dư = 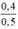 = 0,8 mol/ lit
= 0,8 mol/ lit

\(n_{MnO_2} = \dfrac{4,35}{87} = 0,05(mol)\)
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,05..................................0,05..................(mol)
\(n_{NaOH} = 0,3.0,1 = 0,03(mol)\)
2NaOH + Cl2 → NaCl + NaClO + H2O
0,03........0,05.....0,015.......0,015....................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,015}{0,3} = 0,05M\)

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = = CM(NaClO) =
= 1,6 mol/l
CM(NaOH)dư = = 0,8 mol/l

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = = CM(NaClO) =
= 1,6 mol/l
CM(NaOH)dư = = 0,8 mol/l
500 ml = 0,5l
\(n_{NaOH}=0,5.4=2\left(mol\right)\)
\(n_{MnO_2}=\frac{69,6}{87}=0,8\left(mol\right)\)
a, \(MnO_2+4HCl->MnCl_2+Cl_2+2H_2O\) (1)
\(Cl_2+2NaOH->NaCl+NaClO+H_2O\) (2)
theo (1) \(n_{Cl_2}=n_{MnO_2}=0,8\left(mol\right)\)
vì \(\frac{0,8}{1}< \frac{2}{2}\) => NaOH dư
theo (2) \(n_{NaOH\left(pư\right)}=2n_{Cl_2}=1,6\left(mol\right)\)
=> \(n_{NaOH\left(dư\right)}=2-1,6=0,4\left(mol\right)\)
theo (2) \(n_{NaCl}=n_{Cl_2}=0,8\left(mol\right)\)
nồng độ mol của các chất trọng dung dịch sau phản ứng là
\(C_{M\left(NaCl\right)}=\frac{0,8}{0,5}=1,6M\)
\(C_{M\left(NaOH\right)dư}=\frac{0,4}{0,5}=0,8\left(mol\right)\)

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) =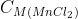 = CM(NaClO) =
= CM(NaClO) =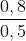 = 1,6 mol/l
= 1,6 mol/l
CM(NaOH)dư =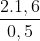 = 0,8 mol/l
= 0,8 mol/l
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
Ta có : nMnO2=69,6/(55+16.2)=0,8 mol
Theo ptpu: nCl2=nMnO2=0,8 mol
nNaOH=0,5.4=2 mol
Cho Cl2 vào dung dịch NaOH
2NaOH + Cl2 -> NaCl + NaClO + H2O
Vì nNaOH > 2nCl2 nên NaOH dư
-> nNaOH phản ứng=2nCl2=0,8.2=1,6 mol
-> nNaOH dư=2-1,6=0,4 mol
nNaCl=nNaClO=nCl2=0,8 mol
->CM NaOH dư=0,4/0,5=0,8M
CM NaCl= CM NaClO=0,8/0,5=1,6M