Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học của phản ứng:
C O 2 + Ca OH 2 → Ca CO 3 + H 2 O
CuO + CO → t ° C O 2 + Cu
Theo phương trình ta có:
n CO 2 = n CaCO 3 = 5/100 = 0,05 mol
n CO = n Cu = 3,2/64 = 0,05 mol
n CaCO 3 = 5/100 = 0,05 mol
n Cu = 3,2/64 = 0,05 mol
Như vậy: n hh = 10/22,4 = 0,45 mol; n N 2 = 0,45 - 0,05 - 0,05 = 0,35 mol
% V N 2 = 0,35/0,45 x 100% = 77,78%
% V CO 2 = % V CO = 0,05/0,45 x 100% = 11,11%
Nếu cho phản ứng (2) thực hiện trước rồi mới đến phản ứng (1) thì
∑ n CO 2 = 0,05 + 0,05 = 0,1 mol
n CaCO 3 = 0,1 mol
Vậy m CaCO 3 = 0,1 x 100 = 10g

Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) (1)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a----------------->a
C2H4 + 3O2 --to--> 2CO2 + 2H2O
b------------------->2b
=> nCO2 = a + 2b (mol)
Do dd sau pư làm quỳ tím chuyển màu xanh
=> Ca(OH)2 dư
\(n_{CaCO_3}=\dfrac{50}{100}=0,5\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,5<-----0,5
=> a + 2b = 0,5 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{C_2H_4}=\dfrac{0,2}{0,3}.100\%=66,67\%\end{matrix}\right.\)

nCaCO3 = 0,1 mol
nH2 = 0,125 mol
Pt: Mg + 2HCl --> MgCl2 + H2
.....0,125 mol<----------------0,125 mol
.....MgCO3 + 2HCl --> MgCl2 + H2O + CO2
.....0,1 mol<----------------------------------0,1 mol
......CO2 + Ca(OH)2 --> CaCO3 + H2O
....0,1 mol<---------------0,1 mol
mA = 0,125 . 24 + 0,1 . 84 = 11,4 (g)
% mMg = \(\dfrac{0,125\times4}{11,4}.100\%=26,3\%\)
% mMgCO3 = \(\dfrac{0,1\times84}{11,4}.100\%=73,7\%\)

\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CO_2}=n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)\\ PTHH:CO+CuO\rightarrow\left(t^o\right)Cu+CO_2\\ n_{CO}=n_{CuO}=\dfrac{40}{80}=0,5\left(mol\right)\\ V_{hh\left(đktc\right)}=\left(n_{CO}+n_{CO_2}\right).22,4=\left(0,5+0,25\right).22,4=16,8\left(l\right)\)

\(Đặt:n_{CH_4}=a\left(mol\right),n_{C_2H_2}=b\left(mol\right)\)
\(n_{hh}=a+b=0.35\left(mol\right)\left(1\right)\)
\(BTC:\)
\(a+2b=0.6\)
\(a=1\)
\(b=0.25\)
\(\%CH_4=\dfrac{0.1}{0.35}\cdot100\%=28.57\%\)
\(\%C_2H_2=71.43\%\)
\(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)⇒ x + y = \(\dfrac{7,84}{22,4} = 0,35(mol)\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_2 + \dfrac{5}{2}O_2 \xrightarrow{t^o} 2CO_2 + H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH : x + 2y = \(\dfrac{60}{100} = 0,6(2)\)
Từ (1)(2) suy ra x = 0,1 ; y = 0,25
Vậy :
\(\%V_{CH_4} = \dfrac{0,1}{0,35}.100\% = 28,57\%\\ \%V_{C_2H_2} = 100\% - 28,57\% = 71,43\%\)
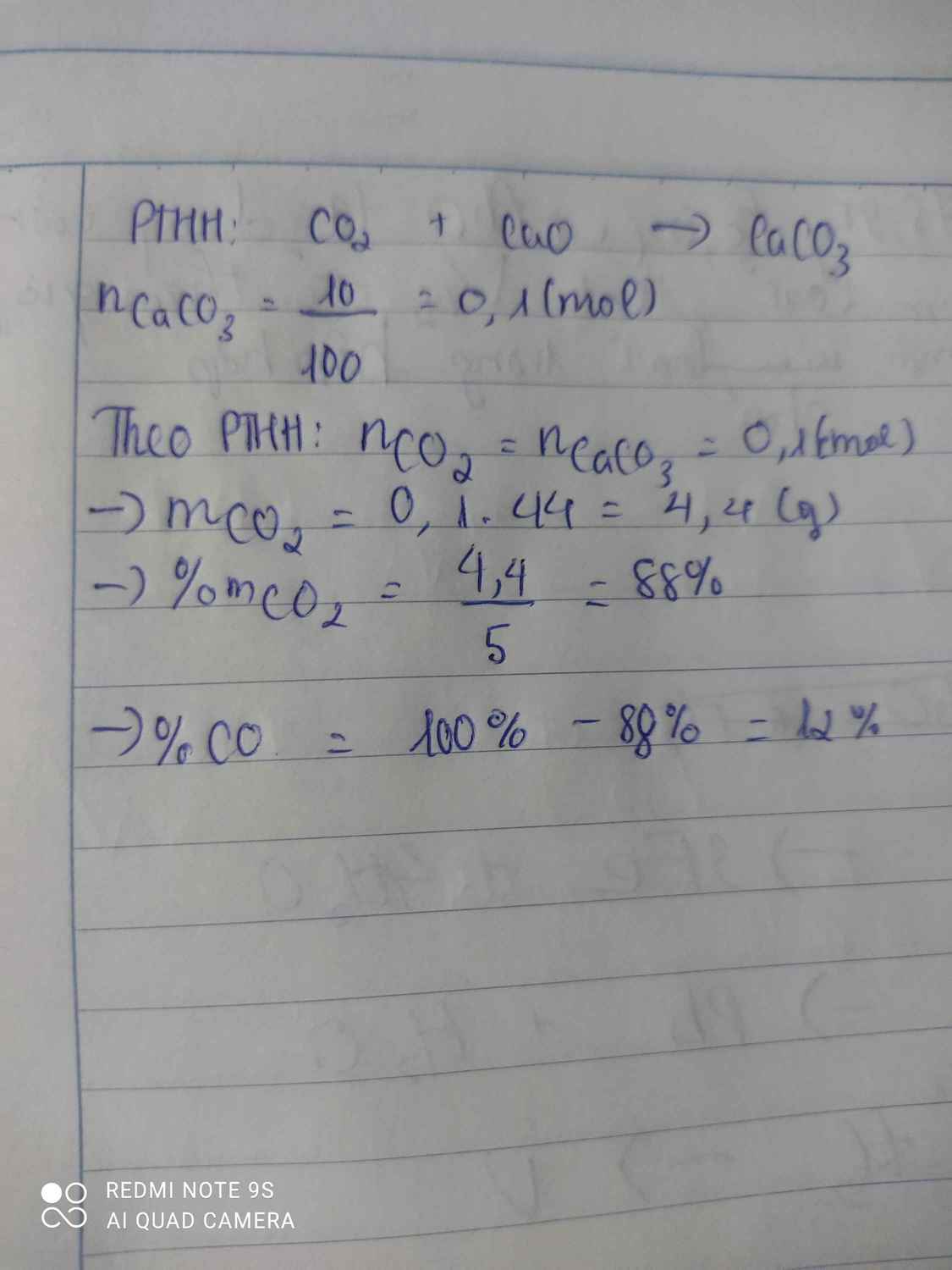
Ta có: \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CO_2}=n_{CaCO_3}=0,1\left(mol\right)\)
\(n_{hh}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
% số mol cũng là % thể tích.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO_2}=\dfrac{0,1}{0,3}.100\%\approx33,33\%\\\%V_{CO}\approx66,67\%\end{matrix}\right.\)