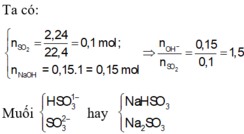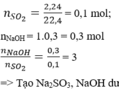Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
\(n_{SO2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{NaOH}=1.0,3=0,3\left(mol\right)\)
\(\frac{n_{NaOH}}{n_{SO2}}=\frac{0,3}{0,25}=1,2\)
Phản ứng tạo 2 muối
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
a_______2a _______ a_______
\(SO_2+NaOH\rightarrow NaHSO_3\)
b_______b__________b
Giải hệ PT:
\(\left\{{}\begin{matrix}a+b=0,25\\2a+b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Na2SO3}=0,05.126=6,3\left(g\right)\)
\(\Rightarrow m_{NaHSO3}=0,2.104=20,8\left(g\right)\)
\(\Rightarrow\Sigma m=20,8+6,3=27,1\left(g\right)\)
Đáp án đúng : A
Cho 5,6 lit khí SO2 (ở đktc) vào 300 ml dung dịch NaOH 1M sau phản ứng thu được m (g) muối. Tìm m= ?

nSO2 = 5,6/22,4 = 0,25 mol, nNaOH = 0,3 mol
Xét tỉ lệ nNaOH/nSO2 = 0,3/0,25 = 1,2
tỉ lệ này nằm trong khoảng 1 đến 2
→ Có hai phản ứng tạo muối xảy ra
(1) SO2 + 2NaOH → Na2SO3 + H2O
a 2a a
(2) SO2 + NaOH → NaHSO3
b b b
Có hệ phương trình: nSO2 = a + b = 0,25
nNaOH = 2a + b = 0,3
→ a = 0,05, b = 0,2
→ mNa2SO3 = 6,3 gam, mNaHSO3 = 20,8 gam
→ m = 6,3 + 20,8 = 27,1 gam
Ta có: \(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{NaOH}=0,3.1=0,3\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{SO_2}}=1,2\)
⇒ Pư tạo 2 muối: NaHSO3 và Na2SO3.
Gọi: \(\left\{{}\begin{matrix}n_{NaHSO_3}=x\left(mol\right)\\n_{Na_2SO_3}=y\left(mol\right)\end{matrix}\right.\)
BTNT Na, S có: \(\left\{{}\begin{matrix}x+2y=0,3\\x+y=0,25\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
⇒ m muối = 0,2.104 + 0,05.126 = 27,1 (g)
Bạn tham khảo nhé!

\(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
nKOH = 0,3.1 = 0,3 (mol)
PTHH: 2KOH + SO2 --> K2SO3 + H2O
0,3-->0,15--->0,15
K2SO3 + SO2 + H2O --> 2KHSO3
0,1<--0,1----------------->0,2
=> hh muối gồm \(\left\{{}\begin{matrix}K_2SO_3:0,05\left(mol\right)\\KHSO_3:0,2\left(mol\right)\end{matrix}\right.\)
=> m = 0,05.158 + 0,2.120 = 31,9 (g)

1) \(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét \(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2S
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,2------------>0,1
=> mNa2S = 0,1.78 = 7,8 (g)
2)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2SO3
PTHH: 2NaOH + SO2 --> Na2SO3 + H2O
0,2-------------->0,1
=> mNa2SO3 = 0,1.126 = 12,6 (g)
2. \(\left\{{}\begin{matrix}n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{NaOH}=0,2.1=0,2\left(mol\right)\end{matrix}\right.\)
Ta có: \(T=\dfrac{0,2}{0,1}=2\) ⇒ tạo ra muối Na2SO3
SO2 + 2NaOH -----> Na2SO3 + H2O

Ta thấy khi cho Br 2 vào dung dịch 2 muối S 4 + thì toàn bộ S 4 + sẽ bị oxi hoá lên S 6 + ( SO 4 2 - )do đó :
n SO 2 = n SO 4 2 - = 0,15
=> m BaSO 4 = 0,15.233 = 34,95g