Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(n_{HCl}=0,5\cdot1=0,5mol\)
PT: \(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(n_R=\dfrac{4,05}{M_R}\)
\(n_{H_2}=\dfrac{5,04}{22,4}=0,225mol\)
\(\Rightarrow\dfrac{4,05}{M_R}\cdot n=0,225\cdot2\)
R là kim loại:
\(\begin{matrix}n&1&2&3\\M_R&9&18&27\end{matrix}\)
Vậy R có hóa trị III và \(M_R=27\left(Al\right)\)
b)PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,15 0,5 0,225
0,15 0,45 0,15 0,225
Vậy \(C_{M_{AlCl_3}}=\dfrac{0,15}{0,5}=0,3M\)

Đáp án B
Gọi ![]() là áp suất riêng phần ban đầu của từng chất khí, ta có :
là áp suất riêng phần ban đầu của từng chất khí, ta có :
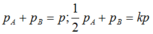
a) từ đó rút ra :
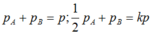
b) Tỉ số mol của hai chất bằng tỉ số áp suất riêng phần ban đầu :
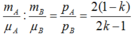
Từ đó rút ra :
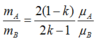
Ap dụng hằng số : 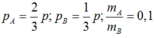

Hình như bạn nhầm nơi rồi đấy đây là BOX Lí mà đăng HÓA

Ta có:
∆E = -4,176.10-13 J = - 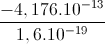 = -2,61 MeV.
= -2,61 MeV.
=> KP = Kn = 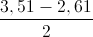 = 0,45 MeV
= 0,45 MeV
Mặt khác ta có:
K = 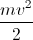 nên v =
nên v = 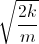 và 931 MeV/u = 1c2
và 931 MeV/u = 1c2
Vậy: vP = 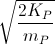 = 1,7.106 m/s.
= 1,7.106 m/s.
m n = 1,0087u
ban đầu có 1 hạt n, sau sinh ra 2 hạt n
=> m hao hụt = m U + m n - m Mo- m La - 2 . m n = 0,23u
=> năng lượng tỏa = 0,23 . 931 = 214 M ev