Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.Ta có n HCl = 1 . 0,25 = 0,25 mol
nH2SO4 = 0,5.0.25 = 0,125 mol
==> nH(X) = 0,25 + 0,125.2 = 0,5 mol
nH2 = 4,368/22,4 = 0,195 mol <=> nH= 0,195. 2 = 0,39 mol < 0,5 mol
Vậy sau phản ứng dung dịch B vẫn còn axit dư
b. Gọi số mol của Al và Mg lần lượt là x và y mol
Ta có phương trình 27x + 24y =3,87 (1)
Áp dụng định luật bảo toàn eletron ==> 3x + 2y = 0,195.2 (2)
Từ (1) , (2) ==> \(\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
mAl = 0,09 .27 = 2,43 gam , %mAl trong A = \(\dfrac{2,43}{3,87}\).100=62,8%
==> %mMg trong A = 100 - 62,8 = 37,2%

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
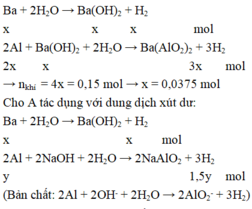

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____3a_______a______\(\dfrac{3}{2}a\) (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
b_____2b_______b______b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+24b=7,8\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,2\cdot27=5,4\left(g\right)\\m_{Mg}=2,4\left(g\right)\\n_{HCl}=0,8\left(mol\right)=n_{H^+}\end{matrix}\right.\)
b) PT ion: \(H^++OH^-\rightarrow H_2O\)
0,8______0,8
Ta có: \(\left[OH^-\right]=C_{M_{NaOH}}+2C_{M_{Ba\left(OH\right)_2}}=2,2\left(M\right)\) \(\Rightarrow V_{OH^-}=\dfrac{0,8}{2,2}\approx0,36\left(l\right)\)

Theo bảo toàn e + đề bài ta có :
\(3x=0,15.2;2y=0,3\)
Với x, y lần lượt là số mol của Al và Cu)
=> x = 0,1 ; y = 0,15 ; => m = 0,1.27 + 0,15.64 = 12,3
Vì Cu đứng sau H trong dãy hoạt động nên ko đẩy đc H khỏi axit nên Cu ko tác tác dụng với HCl nhưng Al thì có(vậy h2 thoát ra là của Al pư)
nH2=3.36/22.4=0.15mol
PTHH: 2Al + 6HCl ---> 2AlCl3 + 3H2
0.1 0.15
m=n*M=>0.1*27=2.7g (1)
Ta biết Al,Fe,Cr thụ động với h2so4 và HNO3 đặc nguội nên trong X chỉ có Cu pư:
nNO2=V*22.4=>6.72/22.4=0.3 mol
PTHH: Cu +4 HNO3 -> Cu(NO3)2 + 2NO2 + 2H2O
0.15 0.3
mCu=0.15*64=9.6g (2)
Từ (1),(2) =>m X =2.7+9.6=12.3g
OH dear,giải xong mệt quá zzzzzzz, chúc em học tốt

Đặt x,y, z lần lượt là số mol của Na,Al,Mg trong m gam hỗn hợp A
m gam A + H2O dư
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
x--------------------x--------->0,5x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x<------x-------------------------------------->1,5x
=> \(0,5x+1,5x=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (1)
2m gam A + NaOH
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
2x------------------------------->x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2y---------------------------------------------->3y
=> \(x+3y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
3m gam A + HCl
\(Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\)
3x--------------------------->1,5x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
3y----------------------------->4,5y
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
3z----------------------------->3z
=> \(1,5x+4,5y+3z=\dfrac{22,4}{22,4}=1\left(mol\right)\) (3)
Từ (1), (2), (3) =>\(\left\{{}\begin{matrix}x=0,05\\y=\dfrac{7}{60}\\z=\dfrac{2}{15}\end{matrix}\right.\)
=> \(m_{Na}=0,05.23=1,15\left(g\right)\)
\(m_{Al}=\dfrac{7}{60}.27=3,15\left(g\right)\)
\(m_{Mg}=\dfrac{2}{15}.24=3,2\left(g\right)\)
=> \(m=1,15+3,15+3,2=7,5\left(g\right)\)
=> \(\%m_{Na}=\dfrac{1,15}{7,5}.100=15,33\%\)
\(\%m_{Al}=\dfrac{3,15}{7,5}.100=42\%\)
\(\%m_{Mg}=\dfrac{3,2}{7,5}.100=42,67\%\)

\(2Na+2H2O\rightarrow2NaOH+H2\left(1\right)\)
\(2Al+2NaOH+2H2O\rightarrow2NaAlO2+3H2\left(2\right)\)
\(2Al+6HCl\rightarrow2AlCl3+3H2\left(3\right)\)
\(2Na+2HCl\rightarrow2NaCl+H2\left(4\right)\)
\(Mg+2HCl\rightarrow MgCl2+H2\left(5\right)\)
\(n_{H2\left(1\right)}=0,1\left(mol\right)\rightarrow n_{Na}=0,2\left(mol\right)\rightarrow m_{Na}=4,6\left(g\right)\)
\(n_{H2\left(2\right)}=0,4\left(mol\right)\Rightarrow n_{Al}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Al}=7,2\left(g\right)\)
\(\Rightarrow n_{H2\left(3\right)}=\dfrac{3}{2}n_{Al}=0,4\left(mol\right)\)
\(n_{H2\left(4\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow n_{H2\left(5\right)}=1-0,4-0,1=0,5\left(mol\right)\)
\(\Rightarrow n_{Mg}=0,5\left(mol\right)\Rightarrow m_{Mg}=12\left(g\right)\)
\(\Rightarrow m=12+4,6+7,2=23,8\left(g\right)\)
\(\%m_{Na}=\dfrac{4,6}{23,8}.100\%=19,33\%\)
\(\%m_{Al}=\dfrac{7,2}{23,8}.100\%=30,25\%\)
\(\%m_{Mg}=100-19,33-30,25=50,42\%\)
Chúc bạn học tốt
a/ Mg(x)+2HCl→MgCl2+H2(x)Mg(x)+2HCl→MgCl2+H2(x)
2Al(y)+6HCl→2AlCl3+3H2(1,5y)2Al(y)+6HCl→2AlCl3+3H2(1,5y)
Giả sử kim loại chỉ có mình Al thì:
nAl=3,8727=43300(mol)nAl=3,8727=43300(mol)
⇒nHCl=43.6300.2=0,43<0,5=nHCl⇒nHCl=43.6300.2=0,43<0,5=nHCl
Giả sử kim loại chỉ có Mg thì
nMg=3,8724=0,16125(mol)nMg=3,8724=0,16125(mol)
⇒nHCl=2.0,16125=0,3225<0,5=nHCl⇒nHCl=2.0,16125=0,3225<0,5=nHCl
Vậy kim loại phản ứng hết HCl dư.
b/ Gọi số mol của Mg và Al lần lược là x, y
⇒24x+27y=3,87(1)⇒24x+27y=3,87(1)
nH2=4,36822,4=0,195(mol)nH2=4,36822,4=0,195(mol)
⇒x+1,5y=0,195(2)⇒x+1,5y=0,195(2)
Từ (1) và (2) ta có hệ: {24x+27y=3,87x+1,5y=0,195{24x+27y=3,87x+1,5y=0,195
⇔{x=0,06y=0,09⇔{x=0,06y=0,09
⇒mMg=0,06.24=1,44(g)⇒mMg=0,06.24=1,44(g)
⇒mAl=0,09.27=2,43(g)