Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{ZnSO_4}=n_{Zn}=0,3\left(mol\right)\Rightarrow m_{ZnSO_4}=0,3.161=48,3\left(g\right)\)
d, \(n_{Fe_2O_3}=\dfrac{64}{160}=0,4\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Mà: H% = 30% \(\Rightarrow n_{H_2\left(pư\right)}=0,3.30\%=0,09\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{2}{3}n_{H_2}=0,06\left(mol\right)\\n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{Fe_2O_3\left(dư\right)}=0,4-0,03=0,37\left(mol\right)\)
\(\Rightarrow a=m_{Fe}+m_{Fe_2O_3\left(dư\right)}=62,56\left(g\right)\)

a, Ta có:
nZn = 13/65= 0,2(mol)
PTHH: Zn + H2SO4 → ZnSO4 + H2
0,2-----------------------------------0,2
Theo PT : nZnSO4 = 0,2.1/1 = 0,2(mol)
mZnSO4 = 0,2. 161 = 32,2(g)
b, Ta có:
Theo PT : nH2 = 0,2.1/1 = 0,2(mol)
VH2(đktc) = 0,2 . 22,4 = 4,48(l)
CuO+H2-to>Cu+H2O
0,2-----0,2
=>m Cu=0,2.64=12,8g
Cậu ơi cho tớ hỏi ngu tý là cái mà "0,2---------0,2" là ntn vậy ạ :"))?

a.b.c.\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,1 0,15 ( mol )
\(V_{H_2}=0,15.22,4=3,36l\)
\(m_{AlCl_3}=0,1.133,5=13,35g\)
d.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,15 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)

$a)Zn + 2HCl \to ZnCl_2 + H_2$
b)
Theo PTHH :
n H2 = n Zn = 1,3/65 = 0,02(mol)
V H2 = 0,02.22,4 = 0,448(lít)
c) $CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
Ta thấy :
n CuO = 2,4/80 = 0,03 > n H2 = 0,02 nên CuO dư
Theo PTHH :
n CuO pư = n Cu = n H2 = 0,02(mol)
Sau phản ứng có :
m Cu = 0,02.64 = 1,28(gam)
m CuO dư = 2,4 - 0,02.80 = 0,8(gam)
Ta có: \(n_{Zn}=\dfrac{1,3}{65}=0,02\left(mol\right)\)
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
_____0,02_________________0,02 (mol)
b, VH2 = 0,02.22,4 = 0,448 (l)
c, Ta có: \(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,03}{1}>\dfrac{0,02}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=n_{H_2}=0,02\left(mol\right)\)
⇒ nCuO (dư) = 0,01 (mol)
\(\Rightarrow m_{CuO\left(dư\right)}=0,01.80=0,89\left(g\right)\)
\(m_{Cu}=0,02.64=1,28\left(g\right)\)
Bạn tham khảo nhé!

a, \(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
b, Theo PT: \(n_{FeSO_4}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{FeSO_4}=0,15.152=22,8\left(g\right)\)
c, \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{CuO\left(dư\right)}=0,3-0,15=0,15\left(mol\right)\)
Chất rắn thu được sau pư gồm Cu và CuO dư.
⇒ m chất rắn = mCu + mCuO (dư) = 0,15.64 + 0,15.80 = 21,6 (g)

\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.n_{Zn}=\dfrac{65}{65}=1\left(mol\right)\\ n_{ZnCl_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=1.136=136\left(g\right)\\ c.n_{H_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow V_{H_2}=1.22,4=22,4\left(l\right)\)

a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,2}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{15}\left(mol\right)\Rightarrow m_{Fe}=\dfrac{2}{15}.56=\dfrac{112}{15}\left(g\right)\)

\(a.n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,2\left(mol\right)\\ m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ V_{H_2}=0,2.22,4=4,48\left(l\right)\\ b.n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\\ CuO+H_2-^{t^o}\rightarrow Cu+H_2O\\ LTL:\dfrac{0,15}{1}< \dfrac{0,2}{1}\\ \Rightarrow H_2dưsauphảnứng\\ n_{Cu}=n_{H_2\left(pứ\right)}=n_{H_2O}=n_{CuO}=0,15\left(mol\right)\\ m_{Cu}=0,15.64=9,6\left(g\right)\\ m_{H_2\left(dư\right)}=\left(0,2-0,15\right).2=0,1\left(g\right)\\ m_{H_2O}=0,15.18=2,7\left(g\right)\)
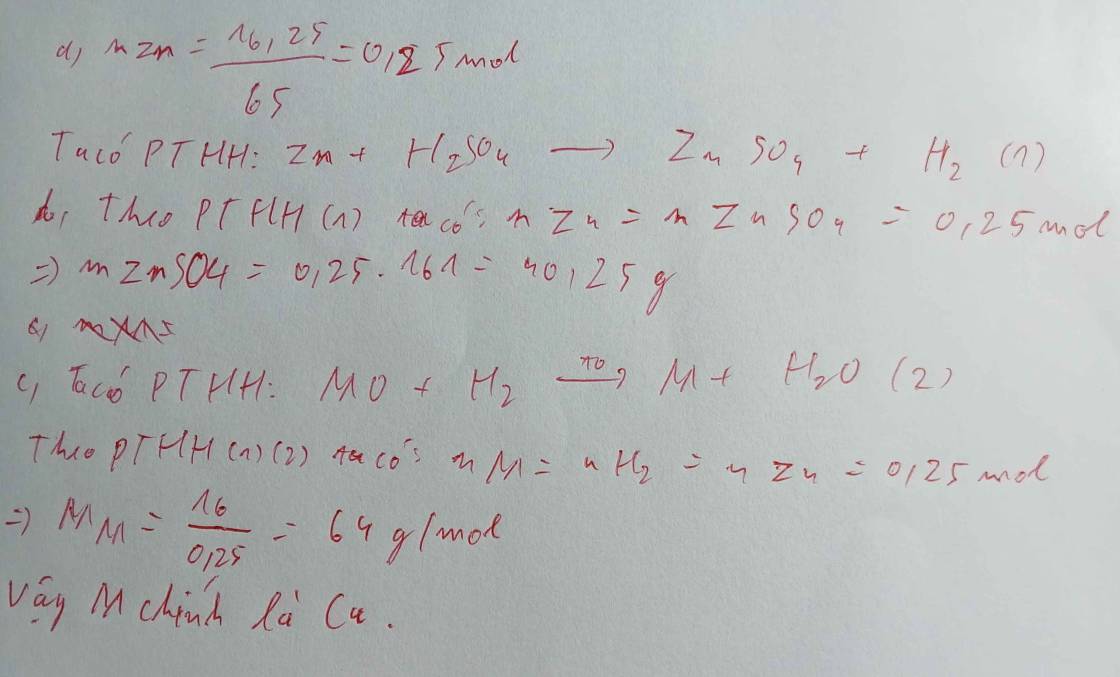
`Zn+H_2SO_4->ZnSO_4+H_2`(to)
0,45-------------------0,45------0,45mol
`n_(Zn)=(29,25)/65=0,45mol`
`m_(ZnSO_4)=0,45.161=72,45g`
`V_(H_2)=0,45.22,4=10,08l`
c) `H_2+CuO->Cu+H_2O`(to)
0,45--------0,45 mol
`n_(Cu)=40/80=0,5 mol`
=>Cu dư , 0,05 mol
`m_(chất rắn)=0,45.64+0,05.80=32,8g`
\(n_{Zn}=\dfrac{m}{M}=\dfrac{29,25}{65}=0,45\left(mol\right)\)
a) \(PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
1 1 1 1
0,45 0,45 0,45 0,45
b) \(m_{ZnSO_4}=n.M=0,45.\left(65+32+16.4\right)=51,03\left(g\right)\\ V_{H_2}=n.24,79=0,45.24,79=11,1555\left(l\right)\)
c) \(n_{CuO}=\dfrac{m}{M}=\dfrac{40}{\left(64+16\right)}=0,5\left(mol\right)\)
\(PTHH:CuO+H_2\rightarrow Cu+H_2O\)
1 1 1 1
0,5 0,5 0,5 0,5
\(m_{Cu}=0,5.64=32\left(g\right).\)