Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

\(n_{Fe}=\dfrac{m}{M}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
1 : 2 : 1 (mol)
0,05 : 0,4 (mol)
-Chuyển thành tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,4}{2}\Rightarrow\) Fe phản ứng hết còn HCl dư.
-Theo PTHH: \(n_{H_2}=\dfrac{0,5.1}{1}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
b) \(n_{Fe\left(cần\right)}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(\Rightarrow n_{Fe\left(thêm\right)}=n_{Fe\left(cần\right)}-n_{Fe\left(tt\right)}=0,2-0,05=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(thêm\right)}=n.M=0,15.56=8,4\left(g\right)\)

1.
a, \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,15 0,3
b, Ta có: \(\dfrac{0,15}{1}< \dfrac{0,5}{2}\) ⇒ Mg pứ hết, HCl dư
\(m_{HCldư}=\left(0,5-0,3\right).36,5=7,3\left(g\right)\)
c, \(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
2.
a, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 ---to→ 2P2O5
Mol: 0,2 0,25 0,1
b, \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c, \(m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(V_{kk}=5,6.5=28\left(l\right)\)

a) Zn + 2HCl --> ZnCl2 + H2
b) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2------------------->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
c) \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,2}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,2<--0,2
=> mCuO(Dư) = (0,3 - 0,2).80 = 8 (g)

\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\\ n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
LTL: \(0,05< \dfrac{0,4}{2}\rightarrow\) HCl dư
Theo pthh: \(\left\{{}\begin{matrix}n_{H_2}=n_{Fe}=0,05\left(mol\right)\\n_{HCl\left(pư\right)}=2n_{Fe}=0,05.2=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}V_{H_2}=0,05.22,4=1,12\left(l\right)\\m_{HCl\left(dư\right)}=\left(0,4-0,1\right).36,5=10,95\left(g\right)\end{matrix}\right.\)
Theo pthh: \(n_{Fe\left(thêm\right)}=\dfrac{1}{2}n_{HCl\left(dư\right)}=\dfrac{1}{2}.\left(0,4-0,1\right)=0,15\left(mol\right)\)
\(\rightarrow m_{Fe\left(thêm\right)}=0,16.56=8,4\left(g\right)\)

mFe= 8,4/56= 0,15 mol
m HCl = 14,6/36,5=0,4 mol
PTHH: Fe +2HCl →FeCl2 +H2
Bđ: 0,15 0,4 0 0 mol
Pứ: o,15→0,3 0,15 0,15 mol
Sau pứ:0 0,1 0,15 0,15 mol
a. HCl dư: m =0,1.36,5=3,65 g
b. m FeCl2 = 0,15.127=19,05 g
c. m H2 = 0,15.2= 0,3 g
V H2= 0,15.22,4=3,36 (l)

\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(m_{HCl}=\dfrac{200\cdot14,6\%}{100\%}=29,2g\Rightarrow n_{HCl}=0,8mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,8 0 0
0,1 0,2 0,1 0,1
0 0,6 0,1 0,1
b)Chất HCl dư và dư \(m=0,6\cdot36,5=21,9g\)
c)\(V_{H_2}=0,1\cdot22,4=2,24l\)
d)\(m_{H_2}=0,1\cdot2=0,2g\)
\(m_{ZnCl_2}=0,1\cdot136=13,6g\)
\(m_{ddZnCl_2}=6,5+200-0,2=206,3g\)
\(C\%=\dfrac{13,6}{206,3}\cdot100\%=6,59\%\)
a, ta có pt sau : Zn + 2HCl >ZnCl2 + H2 (1)
b, nHCl=\(\dfrac{200\times14,6}{100}=29,2\left(g\right)\)\(\Rightarrow n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
Ta có : nZn=\(\dfrac{6,5}{65}=0,1\left(mol\right)\)
Ta có tỉ lệ số mol là : \(\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,1}{1}< \dfrac{0,8}{2}\right)\)
\(\Rightarrow\) HCl dư , Zn pứ hết
Theo pt : nHClpứ = 2.nZn=2.0,1=0,2(mol)
\(\Rightarrow\)nHCl dư = nHCl bđ - nHCl pứ = 0,8 - 0,2 = 0,6 (mol)
\(\Rightarrow\)mHCl dư=0,6.36,6=21,9 (g)
c,theo pt :nH2=nZn=0,1(mol)
\(\Rightarrow\)VH2=0,1.22,4=2,24(l)
d,Các chất có trong dung dịch sau pứ là: ZnCl2 , HCl dư
mk chịu câu này ![]()

\(a,n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right);n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\\ CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\\ Vì:\dfrac{0,1}{1}>\dfrac{0,1}{2}\Rightarrow CaCO_3dư\\ n_{CO_2}=n_{CaCO_3\left(p.ứ\right)}=\dfrac{n_{HCl}}{2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ \Rightarrow n_{CaCO_3\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\\ \Rightarrow m_{CaCO_3\left(dư\right)}=0,05.100=5\left(g\right)\\ b,V_{CO_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)
c) Muốn phản ứng xảy ra vừa đủ, chất nào thiếu ta cần thêm chất đó vào => Cần thêm HCl vào.
\(n_{HCl\left(cần\right)}=2.n_{CaCO_3}=2.0,1=0,2\left(mol\right)\\ \Rightarrow n_{HCl\left(thêm\right)}=0,2-0,1=0,1\left(mol\right)\\ \Rightarrow m_{HCl\left(thêm\right)}=0,1.36,5=3,65\left(g\right)\)
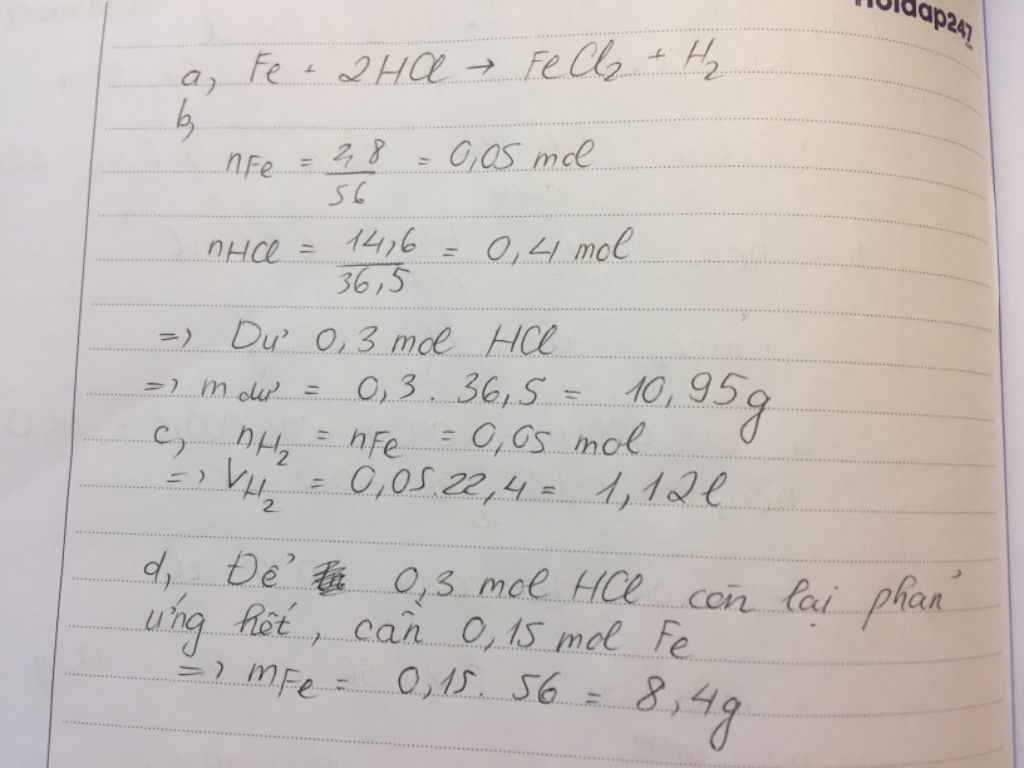

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)