Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`a)`
`Fe + H_2 SO_4 -> FeSO_4 + H_2`
`0,4` `0,4` `0,4` `(mol)`
`n_[Fe]=[22,4]/56=0,4(mol)`
`b)m_[FeSO_4]=0,4.152=60,8(g)`
`c)V_[H_2]=0,4.22,4=8,96(l)`

a) PTHH: Fe + H2SO4 ===> FeSO4 + H2
b) Ta có: nFe = 1456=0,25(mol)1456=0,25(mol)
Theo PTHH, nH2SO4 = nFe = 0,25 (mol)
=> mH2SO4 = 0,25 x 98 = 24,5 (gam)
c) Theo PTHH, nH2 = nFe = 0,25 (mol)
=> VH2(đktc) = 0,25 x 22,4 = 5,6 (l)
d) Theo PTHH, nFeSO4 = nFe = 0,25 (mol)
=> mFeSO4(tạo thành) = 0,25 x 152 = 38 (gam)

a.
n Fe=28562856=0,5 (mol)
Fe+H2SO4→FeSO4+H2↑
0,5→0,5 0,5 0,5 (mol)
b.
V H2(đktc)=0,5.22,4=11,2 (l)
c.
m HCl=0,5.36,5=18,25 (g)
d.
m FeSO4=0,5.152=76 (g)

a)
\(n_{Fe} = \dfrac{14}{56} = 0,25(mol)\)
Phương trình hóa học : \(Fe + H_2SO_4 \to FeSO_4 + H_2\)
Theo PTHH : \(n_{H_2} = n_{Fe} = 0,25(mol)\\ \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)\)
b)
Có : \(n_{H_2SO_4} = n_{H_2} = 0,25(mol)\\ \Rightarrow m_{H_2SO_4} = 0,25.98 = 24,5(gam)\)

PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Ta có: \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{H_2SO_4}=n_{Fe}=0,25\left(mol\right)\)
a, \(V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b, \(m_{H_2SO_4}=0,25.98=24,5\left(g\right)\)
Bạn tham khảo nhé!
nFe = \(\dfrac{14}{56}\)= 0,25 mol
Fe + H2SO4 → FeSO4 + H2
Theo pt : 1 1 1 1 mol
Theo đề bài : 0,25 0,25 0,25 0,25 mol
=> V H2 = 0,25 . 22,4 = 5,6 lít
mH2SO4 = 0,25 . 98 = 24,5 gam

$PTHH:Zn+2HCl\to ZnCl_2+H_2\uparrow$
$n_{Zn}=\dfrac{13}{65}=0,2(mol)$
Theo PT: $n_{ZnCl_2}=n_{H_2}=0,2(mol);n_{HCl}=0,4(mol)$
$a)m_{axit}=m_{HCl}=n.M=0,4.36,5=14,6(g)$
$b)m_{ZnCl_2}=n.M=0,2.136=27,2(g)$
$c)V_{H_2(đktc)}=n.22,4=0,2.22,4=4,48(lít)$
Số mol kẽm là :
\(n=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH : Zn + 2HCL -> ZnCl2 + H2
1 2 1 1
0,2 mol -> 0,4 mol 0,2 mol 0,2 mol
a, Khối lượng HCL là :
\(m=n.M=0,4.35,5=14,2\left(g\right)\)
b, Khối lượng ZnCL2 là :
\(m=n.M=0,1.136=13,6\left(g\right)\)
c, Thể tích H2 là : V = n . 22,4 = \(0,1.22,4=2,24\left(l\right)\)

PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Ta có: \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4}=0,15\left(mol\right)=n_{H_2}\\n_{Al_2\left(SO_4\right)_3}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\\m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\\V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\end{matrix}\right.\)
a) \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
______0,1--->0,15-------->0,05------->0,15
=> mH2SO4 = 0,15.98 = 14,7 (g)
b) VH2 = 0,15.22,4 = 3,36 (l)
c) mAl2(SO4)3 = 0,05.342 = 17,1 (g)

Bài 1
Sắt tác dụng với dung dịch CuSO4 theo phương trình:
Fe + CuSO4 ---------> FeSO4 + Cu
Nếu cho 11,2 g sắt vào 40 g CuSO4. Tính khối lượng Cu thu được sau phản ứng.
----------
1. \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{CuSO_4}=\dfrac{40}{160}=0,25\left(mol\right)\)
Pt: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,2mol 0,25mol \(\rightarrow\) 0,2mol
Lập tỉ số: \(n_{Fe}:n_{CuSO_4}=0,2< 0,25\)
Fe hết, CuSO4 dư
\(m_{Cu}=0,2.64=12,8\left(g\right)\)
Bài 2
Cho sắt tác dụng với dd axit H2SO4 theo sơ đồ sau:
Fe + H2SO4 ---------> FeSO4 + H2
Có 22,4 g sắt tác dụng với 24,5 g H2SO4. Tính:
a) Thể tích khí H2 thu được ở đktc.
b) Khối lượng các chất còn lại sau phản ứng.
------------------------------
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
Pt: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,4mol 0,25mol\(\rightarrow\) 0,25mol\(\rightarrow\)0,25mol
Lập tỉ số: \(n_{Fe}:n_{H_2SO_4}=0,4< 0,25\)
Fe dư, H2SO4 hết
\(V_{H_2}=0,25.22,4=5,6\left(l\right)\)
\(n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
\(m_{FeSO_4}=0,25.152=38\left(g\right)\)
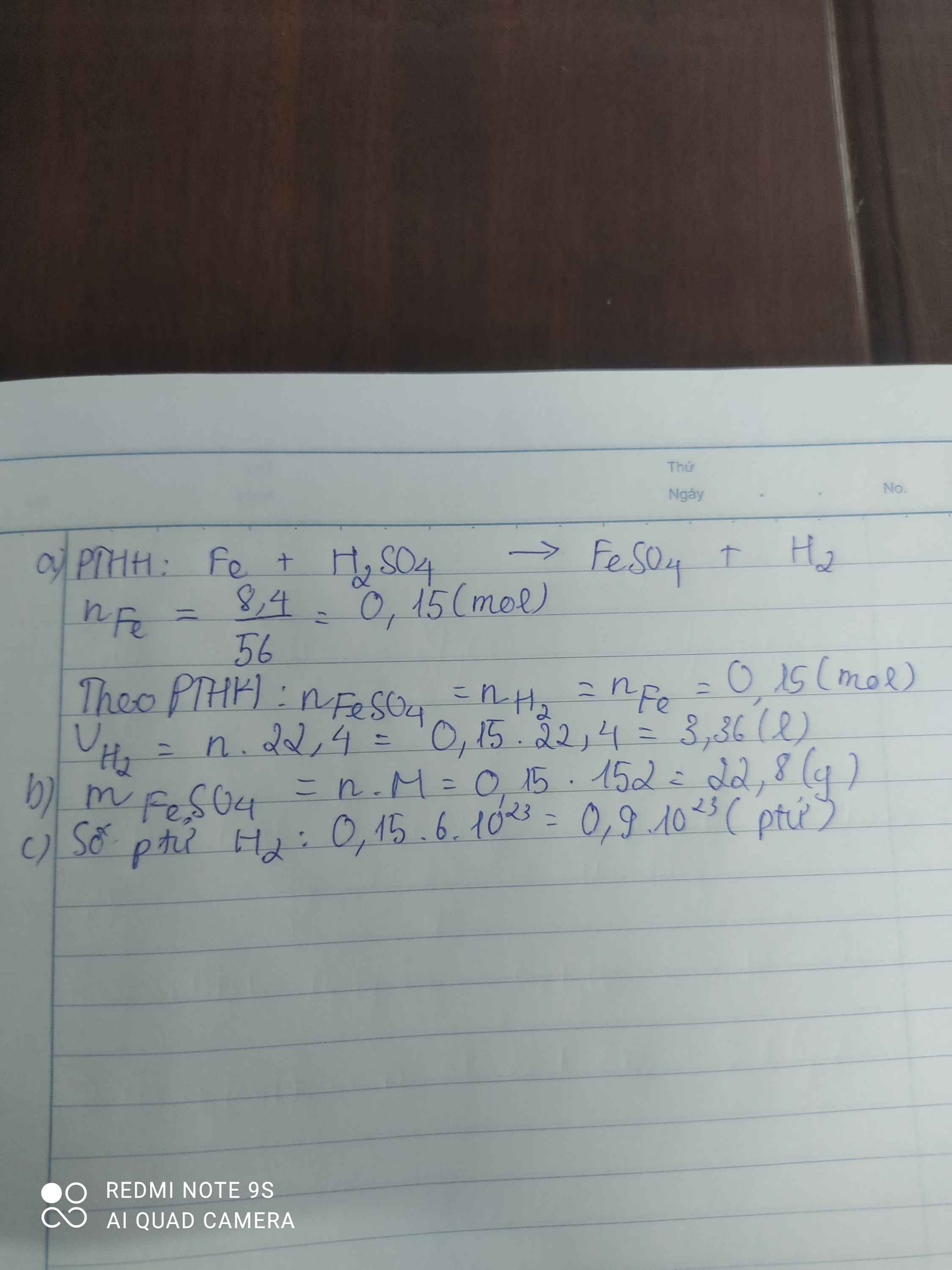
Fe + H2SO4 -> FeSO4 + H2
nFe=0,5(mol)
Theo PTHH ta có:
nFeSO4=nFe=nH2=nH2SO4=0,5(mol)
mFeSO4=152.0,5=76(g)
VH2=22,4.0,5=11,2(lít)
Cách 1:
mH2SO4=98.0,5=49(g)
Cách 2:
Theo ĐLBTKL ta có:
mFe + mH2SO4=mFeSO4+mH2
=>mH2SO4=76+0,5.2-28=49(g)