Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH :
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Trc p/u : 0,4 0,5
p/u: 0,25 0,5 0,25 0,25
sau p/u : 0,15 0 0,25 0,25
b, ----> sau p/ư ; Zn dư
\(m_{Zndư}=0,15.65=9,75\left(g\right)\)
PTHH :
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Từ PTHH ta có , 1 mol Al sẽ cho ra 1,5 mol H2
1 mol Fe sẽ cho ra 1 mol H2
Mà Al lại có Khối lượng mol nhỏ hơn Fe
Vậy , nếu cho cùng 1 khối lượng 2 kim loại trên thì Al sẽ cho ra nhiều H2 hơn

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\n_{HCl}=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) \(\Rightarrow\) HCl còn dư, Kẽm p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,1\left(mol\right)\\n_{HCl\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=22,4\cdot0,1=2,24\left(l\right)\\m_{HCl\left(dư\right)}=0,05\cdot36,5=1,825\left(g\right)\end{matrix}\right.\)

\(a,Zn+2HCl\to ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2(mol);n_{HCl}=\dfrac{21,9}{36,5}=0,6(mol)\)
Vì \(\dfrac{n_{Zn}}{1}<\dfrac{n_{HCl}}{2}\) nên \(HCl\) dư
\(n_{HCl(dư)}=0,6-0,2.2=0,2(mol)\\ c,n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,2(mol)\\ \Rightarrow m_{ZnCl_2}=0,2.136=27,2(g)\\ V_{H_2}=0,2.22,4=4,48(l)\)

Số mol của kẽm
nZn = \(\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,3 0,4 0,2 0,2
a) Lập tỉ số só sánh : \(\dfrac{0,3}{1}>\dfrac{0,4}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
Số mol dư của kẽm
ndư = nban đầu - nmol
= 0,3 - (\(\dfrac{0,4.1}{2}\))
= 0,1 (mol)
Khối lượng dư của kẽm
mdư = ndư . MZn
= 0,1 . 65
= 6,5 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mznCl2 = nZnCl2 . MZnCl2
= 0,2. 136
= 27,2 (g)
c) 4H2 + Fe3O4 → (to) 3Fe + 4H2O\(|\)
4 1 3 4
0,2 0,15
Số mol của sắt
nFe = \(\dfrac{0,2.3}{4}=0,15\left(mol\right)\)
Khối lượng của sắt
mFe = nFe. MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

Zn+2HCl->ZnCl2+H2
0,125-0,25---0,125-0,125
n HCl=\(\dfrac{9,125}{36,5}\)=0,25 mol
=>Zn dư
=>m Zn dư=(0,15-0,125).65=1,625 mol
=>VH2=0,125.22,4=2,8l
=>m ZnCl2=0,125.136=17g
nHCl = 9,125/36,5 = 0,25 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2
LTL: 0,15 > 0,25/2 => Zn dư
nZn (p/ư) = nZnCl2 = nH2 = 0,25/2 = 0,125 (mol)
mZn (dư) = (0,15 - 0,125) . 65 = 1,625 (g)
VH2 = 0,125 . 22,4 = 2,8 (l)
mZnCl2 = 0,125 . 136 = 17 (g)
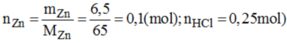
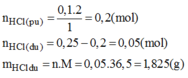

n Zn = 26/65 = 0,4(mol)
$Zn + 2HCl \to ZnCl_2 + H_2$
Ta thấy:
n Zn / 1 = 0,4 > n HCl / 2 = 0,25 nên Zn dư
Theo PTHH :
n Zn pư = 1/2 n HCl = 0,25(mol)
Suy ra: m Zn dư = 26 - 0,25.65 = 9,75 gam
\(n_{Zn}=\dfrac{26}{65}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1........2\)
\(0.4........0.5\)
\(LTL:\dfrac{0.4}{1}>\dfrac{0.5}{2}\Rightarrow Zndư\)
\(m_{Zn\left(dư\right)}=\left(0.4-0.25\right)\cdot65=9.75\left(g\right)\)