Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Phản ứng xảy ra theo thứ tự:
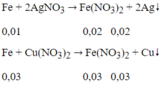
⇒ Fe tan hết
m = 0,02.108 + 0,03.64 = 4,08 (g)

\(Al+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3Ag\left(1\right)\\ n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\Rightarrow n_{AgNO_3\left(1\right)}=3.0,1=0,3\left(mol\right)\\ Fe+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2Ag\left(2\right)\\ n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{AgNO_3\left(2\right)}=0,6-0,3=0,3\left(mol\right)\\ Vì:\dfrac{0,3}{2}< \dfrac{0,2}{1}\Rightarrow Fe.dư\\ Vậy.X:Fe\left(dư\right),Ag\\ n_{Fe\left(dư\right)}=0,2-\dfrac{0,3}{2}=0,05\left(mol\right)\\ n_{Ag}=n_{AgNO_3}=0,6\left(mol\right)\\ m_X=m_{Fe\left(dư\right)}+m_{Ag}=0,05.56+108.0,6=67,6\left(g\right)\)
Anh Pop POP trả lời cho em câu hỏi em mới đăng với nó khó quá ạ

Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
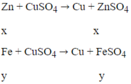
Ta có hệ:
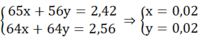
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()

Chọn A.
Ta có: n Y = n H 2 = 0 , 04 m o l mol
=> E gồm các este của ancol (0,04) và các este của phenol (0,08 – 0,04 = 0,04)
mà n H 2 O = n este của phenol = 0,04 mol và n K O H = n este của ancol + 2neste của phenol = 0,12 mol
→ B T K L m E + m K O H = m muối + m ancol + m H 2 O Þ m muối = 13,7 gam

Đáp án A
Sơ đồ phản ứng :
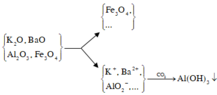
Chất rắn Y có Fe3O4 và có thể còn Al2O3 chưa phản ứng hết. Dung dịch X có có Ba2+, K+, AlO 2 - và có thể có OH - . Sục CO2 dư vào X chỉ thu được kết tủa là Al(OH)3.
Phương trình phản ứng :
![]()
Giả sử trong Y có OH - thì do CO2 có dư nên xảy ra phản ứng :
![]()
Do đó không thể có kết tủa BaCO3.

Chọn A
Chất rắn Y có Fe3O4 và có thể còn Al2O3 chưa phản ứng hết. Dung dịch X có có Ba2+, K+, A l O 2 - và có thể có O H - . Sục CO2 dư vào X chỉ thu được kết tủa là Al(OH)3.

Đáp án C
Phương trình phản ứng:
K2O + H2O → 2KOH
BaO + 2H2O → Ba(OH)2
Al2O3 + OH- → 2AlO2- + H2O
⇒Chất rắn Y: Fe3O4, dung dịch X chứa ion AlO2-
AlO2- + CO2 + H2O → Al(OH)3 + HCO3-

Đáp án C
Al2O3 + 2OH- + 3H2O → 2Al(OH)4-
Al(OH)4- + CO2 → Al(OH)3 + HCO3-

Ở 100°C là nhiệt độ cao bắt buộc ra KClO3
nCl2=0,6 mol
nKCl=0,5 mol
3Cl2 +6KOH =>5KCl + KClO3 +3H2O
0,6 mol
0,3 mol <=0,6 mol 0,5 mol
Dư 0,3 mol
CM dd KOH=0,6/2,5=0,24M
=>Chon A!!!!
Đáp án C
Phản ứng xảy ra theo thứ tự:
⇒ Fe tan hết
m = 0,02.108 + 0,03.64 = 4,08 (g)