Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Từ khối lượng (m) và số mol (n) của kim loại → M = 
- Từ Mhợp chất → Mkim loại
- Từ công thức Faraday → M =  (n là số electron trao đổi ở mỗi điện cực)
(n là số electron trao đổi ở mỗi điện cực)
- Từ a < m < b và α < n < β →  → tìm M thỏa mãn trong khoảng xác định đó
→ tìm M thỏa mãn trong khoảng xác định đó
- Lập hàm số M = f(n) trong đó n là hóa trị của kim loại M (n = 1, 2, 3), nếu trong bài toán tìm oxit kim loại MxOy thì n =  → kim loại M
→ kim loại M

H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g
H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g

Đáp án B
Số mol AlCl3 là nAlCl3= 0,1.1 = 0,1 (mol)
Số mol Al2O3 là nAl2O3= 2,55/102 = 0,025 (mol)
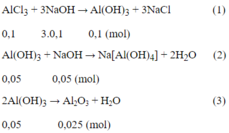
Theo pt (3) ta thấy số mol Al(OH)3 còn lại là 0,05 mol
Như vậy đã có: 0,1 - 0,05 = 0,05 mol Al(OH)3 đã bị hòa tan.
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
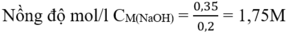

- Coi Fe3O4 là hỗn hợp gồm FeO và Fe2O3
- Như vậy 9,12 gam hỗn hợp gồm FeO và Fe2O3
- Số mol FeCl2=7,62:127=0,06 mol
FeO+2HCl\(\rightarrow\)FeCl2+H2O
Số mol FeO=số mol FeCl2=0,06 mol
Khối lượng Fe2O3=9,12-0,06.72=4,8 gam
Số mol Fe2O3=4,8:160=0,03 mol
Fe2O3+6HCl\(\rightarrow\)2FeCl3+3H2O
Số mol FeCl3=0,03.2=0,06 mol
m=0,06(56+35,5.3)=9,75 g

Đáp án C
Ta có: ![]()
suy ra số mol CO2 trong Z là 0,05 mol tức O bị khử 0,05 mol.
Gọi số mol Fe3O4 và CuO lần lượt là a, b
![]()
Cho Y tác dụng với 1,2 mol HNO3 thu được khí 0,175 mol khí NO2.
Bảo toàn N:
![]()
![]()
Ta có 2 TH xảy ra:
TH1: HNO3 dư.
![]()
![]()
TH2: HNO3 hết.
![]() nghiệm âm loại.
nghiệm âm loại.

Đáp án C
Ta có: n C 6 H 12 O 6 = 1 2 . n Ag = 1 2 . 2 , 16 108 = 0 , 01 mol
→ CM(glucozơ) = n C 6 H 12 O 6 V C 6 H 12 O 6 = 0 , 01 50 . 10 - 3 = 0 , 2 M

Bài 1: Gọi số mol Mg là x, số mol Fe pư là y. số mol Fe dư là z => số mol Cu tạo thành là x + y.
Chất rắn thu được cuối cùng là MgO x mol và Fe2O3 y/2 mol
=> 24x + 56y + 56z = 1,02
64x + 64y + 56z = 1,38.
40x + 80y = 0,9
=> x = y = z = 0,0075 mol.
Vậy, trong A có mMg = 0,0075. 24 = 0,18 g. mFe = 0,0075. 2 . 56 = 0,84g. và CM CuSO4 = 0,0075.2 : 0,2 = 0,075M
Bài 2 tương tự nhé.
24x + 56y + 56z = 12,88.
2x. 108 + 2y. 108 + 56z = 48,72.
40x + 80y = 14.
=> x = 0,07. y = 0,14. z = 0,06

AgNO3 + Hcl -> AgCl + HNO3 (1)
nAgNO3=0,2(mol)
nHCl=0,6(mol)
=> Sau PƯ (1) còn 0,4 mol HCl dư
Từ 1:
nHNO3=nAgCl=nAgNO3=0,2(mol)
mAgCl=143,5.0,2=28,7(g)
C% dd HCl=\(\dfrac{36,5.0,4}{500-28,7}.100\%=3,1\%\)
C% dd HNO3=\(\dfrac{63.0,2}{500-28,7}.100\%=2,67\%\)