Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CuO + 2HCl -> CuCl2 + H2O (1)
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O (2)
nHCl=0,2.3,5=0,7(mol)
Đặt nCuO=a
nFe2O3=b
Ta có hệ:
80a+160b=20
2a+6b=0,7
=>a=0,05;b=0,1
mCuO=80.0,05=4(g)
mFe2O3=20-4=16(g)
Theo PTHH 1 và 2 ta có:
nCuCl2=nCuO=0,05(mol)
nFeCl3=2nFe2O3=0,2(mol)
mCuCl2=135.0,05=6,75(g)
mFeCl3=162,5.0,2=32,5(g)
mdd =20+200.1,1=240(g)
C% dd CuCl2=6,72\240 .100%=2,8125%
C% dd FeCl3= 32,5\240 .100%=13,54%

Đổi 200ml = 0,2 lít
Ta có: \(n_{HCl}=3,5.0,2=0,7\left(mol\right)\)
Gọi x, y lần lượt là số mol của CuO và Fe2O3
PTHH:
CuO + 2HCl ----> CuCl2 + H2O (1)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O (2)
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Fe_2O_3}=6y\left(mol\right)\)
=> 2x + 6y = 0,7 (*)
Theo đề, ta có: 80x + 160y = 20 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+160y=20\end{matrix}\right.\)
=> x = 0,05, y = 0,1
=> \(m_{CuO}=80.0,05=4\left(g\right)\)
\(m_{Fe_2O_3}=20-4=16\left(g\right)\)
đổi 200ml = 0.2 l
nhcl = 0.2*3.5 = 0.7 ( mol)
gọi số mol của CuO là x
số mol của Fe2O3 là y
PTHH:
CuO + 2HCl ➜ CuCl2 + H2O
x 2x
Fe2O3 + 6HCl ➜ 2FeCl3 + 3H2O
y 6y
ta có hệ phương trình
\(\left\{{}\begin{matrix}80x+160y=20\\2x+6y=0,7\end{matrix}\right.\)
⇒ x= 0.05
y=0.1
mCuO= 0.05*80=4 (g)
mFe2O3= 0.1*160=16(g)

Đặt : \(n_{CuO}=a\left(mol\right),n_{ZnO}=b\left(mol\right)\)
\(\Rightarrow80a+81b=28,25g\left(1\right)\)
a) Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
b) Ta có : \(n_{HCl}=\dfrac{20\%.127,75}{100\%.36,5}=0,7\left(mol\right)\Rightarrow2a+2b=0.7\left(2\right)\)
Từ (1),(2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1=n_{CuCl2}\\b=0,25=n_{ZnCl2}\end{matrix}\right.\)
c) \(m_{muối}=m_{CuCl2}+m_{ZnCl2}=0,1.135+0,25.136=47,5\left(g\right)\)
d) \(\left\{{}\begin{matrix}C\%_{CuCl2}=\dfrac{0,1.135}{28,25+127,75}.100\%=8,65\%\\C\%_{ZnCl2}=\dfrac{0,25.136}{28,25+127,75}.100\%=21,79\%\end{matrix}\right.\)

\(n_{Al_2O_3}=a\left(mol\right)\)
\(n_{MgO}=b\left(mol\right)\)
\(m_A=102a+40b=16.2\left(g\right)\left(1\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(m_{Muối}=267a+111b=40.95\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.249,b=-0.23\)
Sai đề !

a. PTHH:
CuO + HCl ---x--->
Al2O3 + 6HCl ---> 2AlCl3 + 3H2O
b. Đổi 100ml = 0,1 lít
Ta có: \(n_{HCl}=7.0,1=0,7\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{6}.n_{HCl}=\dfrac{1}{6}.0,7=\dfrac{7}{60}\left(mol\right)\)
=> \(m_{Al_2O_3}=\dfrac{7}{60}.102=11,9\left(g\right)\)
=> \(m_{CuO}=21,1-11,9=9,2\left(g\right)\)
Sửa:
a. PTHH:
CuO + 2HCl ------> CuCl2 + H2O (1)
Al2O3 + 6HCl ---> 2AlCl3 + 3H2O (2)
b. Đổi 100ml = 0,1 lít
Ta có: \(n_{HCl}=7.0,1=0,7\left(mol\right)\)
Gọi x, y lần lượt là số mol của CuO và Al2O3
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Al_2O_3}=6y\left(mol\right)\)
=> 2x + 6y = 0,7 (*)
Theo đề, ta có: 80x + 102y = 21,1 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+102y=21,1\end{matrix}\right.\)
=> x = 0,2, y = 0,05
=> \(m_{CuO}=80.0,2=16\left(g\right)\)
\(m_{Al_2O_3}=21,1-16=5,1\left(g\right)\)

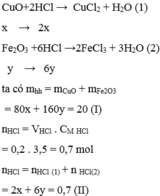
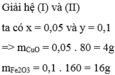
CuO + 2HCl → CuCl2 + H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
\(n_{HCl}=0,2\times3,5=0,7\left(mol\right)\)
Gọi x,y lần lượt là số mol của CuO và Fe2O3
Ta có: \(80x+160y=20\) (*)
Theo PT1: \(n_{HCl}=2n_{CuO}=2x\left(mol\right)\)
Theo pT2: \(n_{HCl}=6n_{Fe_2O_3}=6y\left(mol\right)\)
Ta có: \(2x+6y=0,7\) (**)
Từ (*)(**) ta có: \(\left\{{}\begin{matrix}80x+160y=20\\2x+6y=0,7\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
Vậy \(n_{CuO}=0,05\left(mol\right)\Rightarrow m_{CuO}=0,05\times80=4\left(g\right)\)
\(n_{Fe_2O_3}=0,1\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,1\times160=16\left(g\right)\)
Đặt:
nCuO= x mol
nFe2O3= y mol
mhh= 80x + 160y= 20 g (1)
nHCl= 0.2*3.5=0.7 mol
CuO + 2HCl --> CuCl2 + H2O
x_______2x
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
y________6y
nHCl= 2x + 6y = 0.7(2)
Giải (1) và (2) :
x= 0.05
y= 0.1
mCuO= 0.05*80=4
mFe2O3= 0.1*160=16g