Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
\(H_2+Cl_2\rightarrow2HCl\left(1\right)\)
___0,03______0,06
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\)
\(n_{AgCl}=\frac{0,17}{108+35,5}\)
\(n_{HCl\left(1\right)}=\frac{0,17}{108+35,5}.\frac{20}{5}=\frac{34}{7175}\)
\(n_{H2}=\frac{1}{22,4}\)
\(n_{Cl2}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
\(\Rightarrow H=\frac{\frac{34}{7145}}{0,06}.100\%=7,9\%\)
Câu 3:
\(n_{NaCl}=\frac{12,87}{23+35,5}=0,22\left(mol\right)\)
\(2NaCl+H_2SO_4\rightarrow Na_2SO_4+2HCl\)
0,22____________0,11___________0,22
\(n_{NaCl}=n_{HCl}=0,22\left(mol\right)\)
\(\Rightarrow V_{HCl}=0,22.22,4.90\%=4,43521\)
\(m_{Na2SO4}=0,11.142.90\%=14,058\left(g\right)\)

Bài 1:
Giả sử 2 muối NaX và NaY đều cho kết tủa:
Ta có
\(NaM+AgNO_3\rightarrow AgX+NaNO_3\)
\(m_{tang}=\left(108-23\right).nM=8,61-6,03\)
\(\rightarrow n_M=0,03\left(mol\right)\)
\(M_M=\frac{6,03}{0,03-23}=175,6\)
Không có một halogen nào thỏa mãn.
Phải có một muối là NaF (AgF không kết tủa), vì là 2 halogen thuộc 2 chu kì liên tiếp nên Y là Cl
\(n_{AgCl}=\frac{8,61}{143,5}=0,06\left(mol\right)\)
\(\rightarrow n_{NaCl}=0,06\left(mol\right)\)
\(\rightarrow m_{NaF}=6,03-0,06.58,5=2,52\left(g\right)\)
\(\%m_{NaF}=\frac{2,52}{6,03}.100\%=41,79\%\)
Bài 2:
Spu, \(m_{giam}=m_{Br^-}-m_{Cl}=1,6-1,155=0,445\left(mol\right)\)
Gọi x là mCl- thì x+0,445 là mBr-
\(Cl_2+2Br^-\rightarrow Br_2+2Cl^-\)
\(\rightarrow n_{Cl^-}=n_{Br^-}\)
\(\Leftrightarrow\frac{x}{35,5}=\frac{x+0,445}{80}\)
\(\rightarrow35,5.\left(x+0,445\right)=80x\)
\(\Leftrightarrow x=0,355\)
\(n_{Cl^-}=\frac{0,335}{35,5}\left(mol\right)\)
\(\rightarrow n_{Cl2}=\frac{0,335}{71}\left(mol\right)\)
\(\rightarrow m_{Cl2}=0,335\left(g\right)\)
\(\%_{Cl2}=\frac{0,335.100}{5}=6,7\%\)
Bài 4:
Chất ko tan là Cu
\(\rightarrow m_{Mg,Al}=10,14-6,4=3,74\left(g\right)\)
\(n_{H2}=0,35\left(mol\right)\)
\(\rightarrow n_{HCl}=2n_{H2}=0,7\left(mol\right)=n_{Cl}\)
\(\rightarrow m_{Cl}=24,85\left(g\right)\)
\(m_{muoi}=3,75+24,85=29,59\left(g\right)\)

Bài 1. Bài làm:
\(n_{H_2}=\frac{1}{22,4}=0,0446mol;n_{Cl_2}=0,03mol\)
H2 + Cl2 → 2HCl (1)
Vì \(n_{H_2}>n_{Cl_2}\Rightarrow\) hiệu suất phản ứng tính theo Cl2
AgNO3 + HCl → AgCl + HNO3
⇒ nHCl (trong 5g A) = nAgCl = 0,01 mol
⇒ nHCl (trong 20g A) = 0,01.4 = 0,04 mol
Từ (1)⇒ \(n_{Cl_2}\)phản ứng = 0,5.nHCl = 0,5.0,04 = 0,02 mol
⇒ H% = \(\frac{0,02}{0,03}\) .100% = 66,67%
Bài 2. Bài làm:
Dung dịch Y chỉ chứa KCl: 0,8mol → số mol HCl: 0,8mol
→ mddHCl\(=\frac{0,8.36,5}{0,146}=200gam\)
Khối lượng dung dịch Y là: mdd Y\(=\frac{59,6}{0,250841}=237,6gam\)
Bảo toàn khối lượng → \(m+200=237,6+15.2.0,3\rightarrow m=46,6gam\)

nBr2=0,05 mol
SO2 + Br2 + H2O =>H2SO4 +2HBr
0,05 mol<=0,05 mol
Chỉ có Cu pứ vs H2SO4 đặc nguội
Cu =>Cu+2 +2e
0,05 mol<= 0,1 mol
S+6 +2e =>S+4
0,1 mol<=0,05 mol
=>nCu=0,05 mol=>mCu=3,2g
=>mAl=5,9-3,2=2,7g
=>nAl=0,1 mol
Tổng nhh cr=0,1+0,05=0,15 mol

a/ PTHH: R + 2HCl ===> RCl2 + H2
nH2 = 2,688 / 22,4 = 0,12 (mol)
nR = nH2 = 0,12 mol
=> MR = 6,72 / 0,12 = 56 (g/mol)
=> R là Fe

Đáp án:
8,625 g
Giải thích các bước giải:
nCl2=22,4/22,4=1 mol
nNaOH=0,1x2=0,2 mol
nCa(OH)2=0,1x0,5=0,05 mol
2NaOH+Cl2->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2+2Cl2->CaCl2+Ca(ClO)2+2H2O
0,05 0,05 0,025
m=0,025x111+0,1x58,5=8,625 g
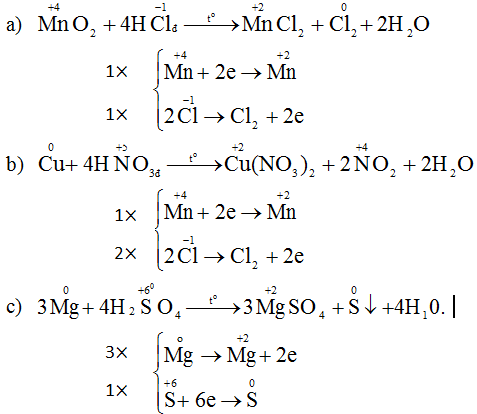

Đáp án là B. 80%